过去的十年间,肿瘤免疫治疗取得飞速发展,深远地革新了肿瘤治疗模式。然而,较低的患者应答率(10%~30%)和潜在的免疫副作用仍然是肿瘤免疫治疗最大的临床挑战。抗肿瘤纳米药物具有可控的递送和可调的模块化功能,为强化抗肿瘤免疫应答及增强肿瘤对免疫治疗的敏感度提供了契机。特别的,肿瘤微环境响应纳米药物可以通过安全有效的方式实现肿瘤组织免疫反应特异性及局域性的放大,从而在提高患者对免疫治疗应答率的同时降低免疫相关副反应。因此,肿瘤微环境响应纳米药物已成为增强癌症免疫治疗的一个很有前途的研究方向。
近期,四川大学高会乐教授课题组在这一领域开展了系统的研究工作,利用肿瘤微环境高表达的酶、高浓度的谷胱甘肽及弱酸性等,设计了一系列肿瘤微环境响应纳米药物,用于增强抗肿瘤免疫治疗 (Adv. Funct. Mater., 2019, 29,1901896; Nano Lett., 2019, 19, 8318; Sci. Adv., 2021, 7, eaba0776; Adv. Funct. Mater., 2021, 31, 2104645) 最近,高会乐教授受邀在Advanced Science上发表相关综述性文章。
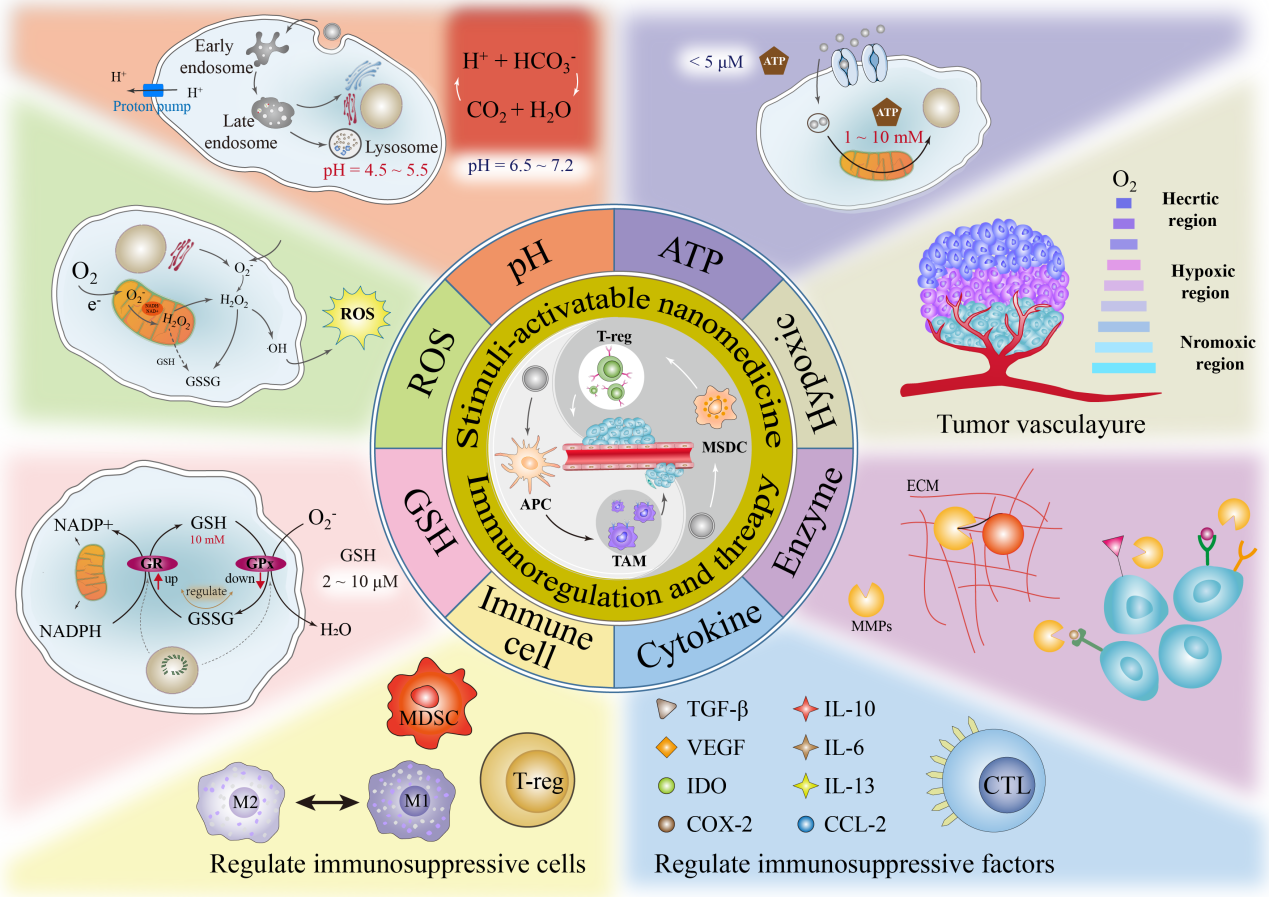
该综述首先系统介绍了肿瘤微环境呈弱酸、高浓度谷胱甘肽、高浓度活性氧、高表达的酶、乏氧及高浓度的三磷酸腺苷等特征。综述从不同的刺激响应及多种刺激响应组合出发对当前用于增强免疫治疗的肿瘤微环境响应纳米药物进行了系统总结。综述最后还对目前肿瘤微环境响应纳米药物应用于免疫治疗存在的问题和临床瓶颈进行了探讨,也对其未来潜在的应用进行了展望。
相关研究成果近期发表在ADVANCED SCIENCE上(DOI: 10.1002/advs.202103836, IF=16.806)。该工作得到了国家自然科学基金和中国科协青年人才托举工程等的资助。暨南大学附属珠海医院彭绍军副研究员为第一兼共同通讯作者,高会乐教授为最后通讯作者。
论文链接:https://doi.org/10.1002/advs.202103836
- 常州大学王建浩教授团队 IJBM:负载鱼腥草囊泡的微环境响应胶原水凝胶治疗糖尿病伤口的研究成果 2025-07-14
- 浙大傅国胜/黄翯/赵静《ACS Nano》:可喷涂微环境响应型水凝胶涂层重塑内皮屏障稳态,破解介入后再狭窄难题 2025-06-04
- 上海市第一人民医院马小军/东华大学何创龙 Bioact. Mater.:TME响应复合水凝胶靶向抑制MYC驱动型骨肉瘤生长与转移 2025-01-17
- 东华大学史向阳教授团队 Bioact. Mater.:全活性含磷树冠大分子纳米药物通过多靶点免疫调控与神经保护缓解缺血性脑卒中 2026-04-10
- 海南大学吴锡龙教授 AFM:聚焦纳米药物瘤内穿透难题 - 以超声/磁场双引擎驱动实现S型异质结纳米晶的深层肿瘤消融与免疫激活 2026-03-26
- 北京化工大学王兴教授团队《Adv.Healthc.Mater.》:基于双抗生素的pH响应型无载体纳米药物高效治疗混合细菌感染 2025-08-11
- 华南理工朱伟、北化工郭佶慜、新墨西哥大学Brinker教授 PNAS:针对肿瘤异质性的全细胞疫苗 2026-04-08
