癌症已成为人类生命健康的一个重大威胁,肿瘤转移是影响肿瘤治疗预后的关键因素。由于肿瘤的转移和侵袭特性,肿瘤细胞可以从原位肿瘤脱落进入血液循环系统,成为循环肿瘤细胞(CTCs),进一步形成远端肿瘤病灶甚至通过血流扩散至全身。当远端转移发生时,大多数治疗效果有限,预后极差。因此,抑制肿瘤的转移和侵袭是改善肿瘤治疗的关键。尽管全身化疗对CTCs具有一定的杀伤作用,但由于化疗药物的毒副作用,其治疗效果非常有限。换言之,一旦形成CTCs,就很难有效地清除。从根本上减少肿瘤细胞的脱落对于有效预防肿瘤转移至关重要,因此亟需开发一种新型的肿瘤治疗平台在治疗原位肿瘤的同时有效抑制肿瘤细胞的脱落。
静电纺纳米纤维具有比表面积大、易于制备和功能化修饰等优点,可以在纳米纤维表面修饰靶向配体,用于特异性捕获癌细胞。在前期的研究中,史向阳教授团队利用叶酸或者透明质酸功能化修饰的纳米纤维膜,可静态捕获叶酸受体高表达或者CD44受体高表达的癌细胞(J. Mater. Chem. B 2014, 2, 7384-7393; Adv. Mater. Interfaces 2015, 2, 1500256)。进一步地,课题组将靶向配体功能化的纳米纤维膜结合微流控技术,获得整合纳米纤维的微流控芯片,实现了多种癌细胞的高效、特异性动态捕获和无损分离(Mater. Chem. Front. 2018, 2, 891-900; Bioconjugate Chem. 2018, 29, 1081-1090; Nanomedicine 2019, 14, 183-199)。DNA适配体,作为一种单链寡核苷酸序列,可以特异性结合细胞膜上的受体,其亲和力与抗体相当甚至更高。由于DNA适配体本身带负电荷,很少涉及与细胞的非特异性相互作用,因此具有很高的靶向特异性。此外,DNA适配体具有良好的生物相容性、稳定性、易于制备和表面修饰等优点,可以作为一种理想的靶向配体用于癌细胞的特异性捕获。基于此,他们推测DNA适配体功能化的纳米纤维有望成为抑制CTCs脱落的一个有力工具。
传统静电纺纳米纤维通常以纤维膜的形式用作敷料或者组织工程支架,这极大地限制了其在生物医学领域的应用。最近的研究表明,静电纺纳米纤维可以通过冷冻切片或均质化处理加工成单分散短纤维,从而实现纳米纤维的可注射化。史向阳教授团队前期通过静电纺丝和均质破碎处理制备了内部负载磁性四氧化三铁的单分散纳米短纤维,并在纤维表面修饰DNA适配体作为靶向分子,用于肿瘤细胞的高效捕获和分离(Bioconjugate Chem. 2020, 31, 130-138)。
癌症化疗药物往往存在毒副作用大、作用时间短和生物利用度低等问题。聚乳酸-羟基乙酸(PLGA)具有优异的生物相容性和生物降解性。研究证实,利用PLGA纳米纤维负载抗菌或者抗癌药物可以实现药物的长效稳定缓释(ACS Appl. Mater. Interfaces 2012, 4, 6393-6401; Biomaterials 2013, 34, 1402-1412; Polym. Chem. 2013, 4, 933-941)。此外,通过调节PLGA的降解周期可以获得预期的药物释放行为。因此,PLGA纳米纤维可用作长效化疗的理想药物载体。
在上述研究的基础上,史向阳教授团队联合东华大学材料科学与工程学院朱美芳院士、上海市第一人民医院刘勇教授提出了一种基于多功能载药PLGA纤维环的新策略,通过从源头上减少肿瘤细胞脱落,在治疗原位肿瘤的同时抑制肿瘤转移。在本研究中,课题组首先制备了静电纺PLGA纳米纤维膜,随后将纤维膜剪成碎片,并在含有不同浓度NaCl的聚乙烯醇(PVA)水溶液中均质处理以制备纳米短纤维,尝试在高离子强度下利用聚合物纤维在水溶液中的形变性制备弯曲的短纤维。结果显示,盐浓度会显著影响PLGA短纤维的形态(图1):在无NaCl的水溶液中均质处理后获得短纤维;在浓度为1 M的盐溶液下形成具有一小部分纤维环的弯曲短纤维;当盐浓度增加到2 M时,产物大多为纤维环;当盐浓度进一步增加至3~4 M时,则形成螺旋形纤维。显然,在NaCl存在下,PLGA短纤维显示出增强的柔韧性和形变性,这极大地促进了纤维环的形成。
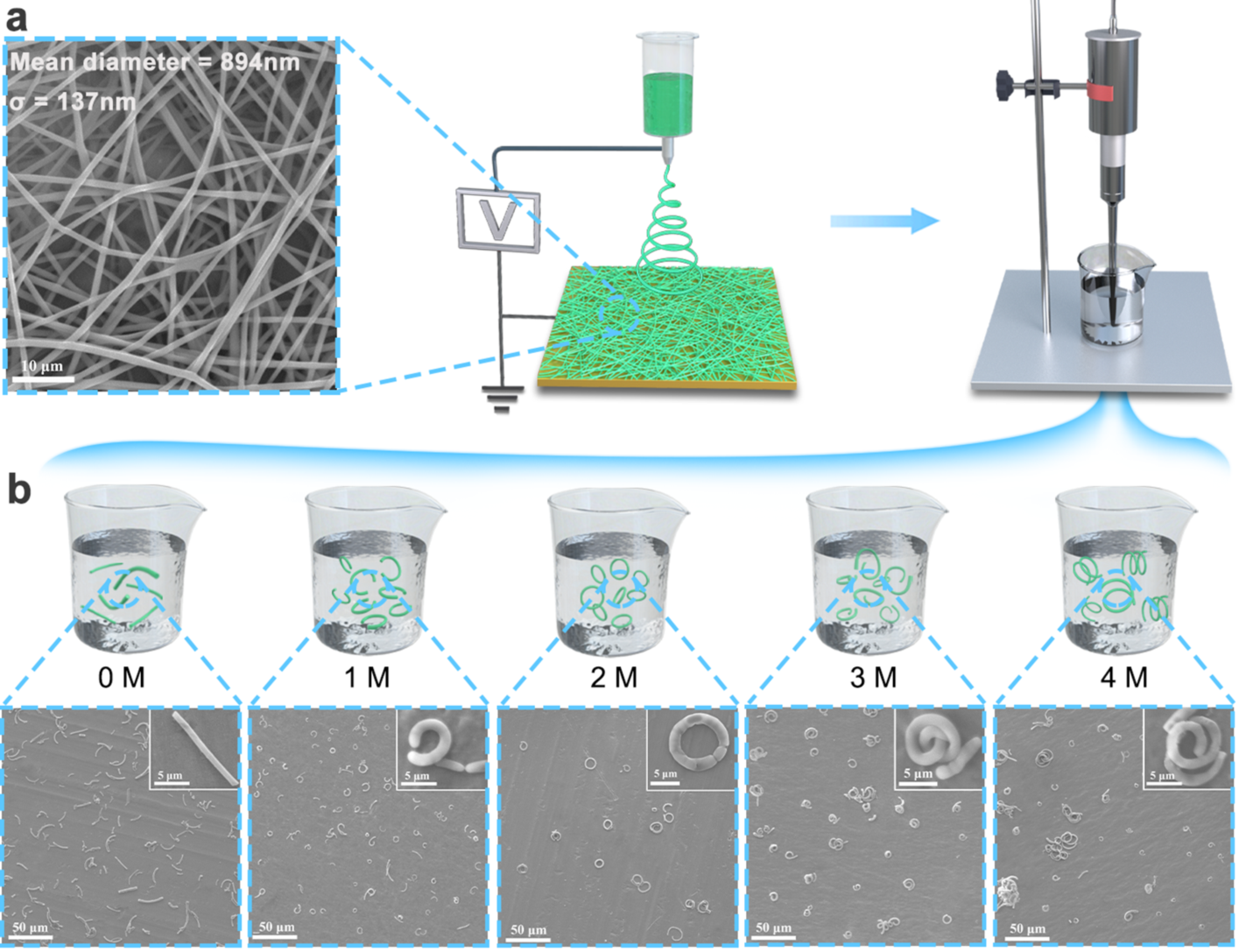
图1. (a)静电纺PLGA纤维环的制备过程以及(b)在不同浓度(0 M、1 M、2 M、3 M和4 M)NaCl溶液中PLGA纤维膜经均质处理后得到的纤维片段的SEM形貌。
在制备了PLGA纤维环的基础上,研究组进一步对其进行功能化处理,用于肿瘤化疗及抑制肿瘤转移(图2)。首先,在优化的盐浓度和均质时间条件下,通过静电纺丝和均质工艺获得负载阿霉素的PLGA纤维环(DOX@PLGA)。之后,以超支化聚乙烯亚胺(PEI)作为中间连接体将Gd(III)螯合到DOX@PLGA纤维环的表面用以磁共振(MR)成像,然后连接DNA适配体作为靶向分子。制备的多功能PLGA纤维环具有长期稳定的药物缓释特性,可用于肿瘤的长效化疗;功能化纤维环的环状结构和DNA适配体介导的靶向结合作用为纤维环提供了强大的结合力,使其能够有效锚定肿瘤细胞,减少肿瘤细胞的脱落,并延长其在肿瘤部位的滞留时间,MR成像结果显示,即使在原位注射后一周内,肿瘤部位仍显示较强的MR信噪比。动物实验结果表明,制备的功能化载药PLGA纤维环能够长效抑制肿瘤,并通过减少CTCs的形成有效抑制肿瘤转移。构建的多功能载药纤维环可以有效治疗原发瘤的同时抑制肿瘤转移,在癌症诊疗应用方面具有较大潜力。

图2. 载药PLGA纤维环的制备、表面修饰及其在肿瘤诊疗和抗转移应用示意图。
以上研究成果以Multifunctional PLGA microfibrous rings enable MR imaging-guided tumor chemotherapy and metastasis inhibition through prevention of circulating tumor cell shedding为题,发表于国际知名期刊Nano Today(Nano Today 38 (2021) 101123, DOI:10.1016/j.nantod.2021.101123)。东华大学化学化工与生物工程学院博士生肖云超和范钰为论文共同第一作者,史向阳教授与上海市第一人民医院肿瘤放疗科刘勇教授为共同通讯作者。该工作得到了国家自然科学基金委、上海市科委项目等项目的资助。
文章链接:https://www.sciencedirect.com/science/article/abs/pii/S1748013221000487
- 中国矿业大学 Nat. Commun.:深地深空复杂条件微环境管理多级异质界面纳纤 2026-05-15
- 杭师大朱雨田教授、陈建闻副教授/南开刘遵峰教授 AFM:连续静电纺丝核鞘摩擦电纳米纱线 - 无缝集成的高输出多功能传感材料 2025-11-25
- 北京纳米能源所董凯团队 Adv. Mater.:提高半晶生物聚合物机电转换性能的通用取向工程策略 2025-08-19
- 东华大学朱美芳/成艳华团队 Adv. Mater.:轻质热防护材料助力空间离轨与柔性舱展开系统 2026-06-02
- 苏州大学汪晓巧教授、张克勤教授团队 ACS Nano:兼具辐射制冷与空气过滤双功能的螺旋纳米纤维膜 2026-04-30
- 武汉纺织大学王桦/王罗新团队熊思维 AFM:聚芳酯纳米纤维气凝胶蜂窝的热-声-力耦合机制 - 骨架阻隔与芯层耗散协同作用 2026-04-23
- 四川大学高会乐教授课题组 ACS Nano: 甘露糖纳米粒搭乘GLUT1受体循环克服口服入脑多重屏障用于阿尔茨海默症的联合治疗 2024-01-16
