除了一些实验性绷带外,大多数绷带通常只是用于覆盖伤口,而不是积极治愈伤口。然而,新的“活性粘合剂敷料”(AAD)绷带并非如此,其在模仿胚胎皮肤的同时放弃了抗生素的使用。
在动物胚胎的发育过程中,胚胎在伤口愈合时皮肤不会留下疤痕。这是因为这些伤口周围的皮肤细胞产生由称为肌动蛋白的蛋白质制成的纤维。这些纤维收缩,从而通过将其边缘拉在一起来愈合伤口,其不会产生疤痕组织。
哈佛大学与麦吉尔大学的研究人员合作,开始通过复制这个过程来研发全新的绷带。得到的AAD由粘合剂藻酸盐(藻类衍生的)水凝胶制成,其上已加入银纳米颗粒和称为PNIPAm的热响应聚合物。该聚合物不仅具有疏水性,而且还可以在约90oF(32oC)的温度下收缩。
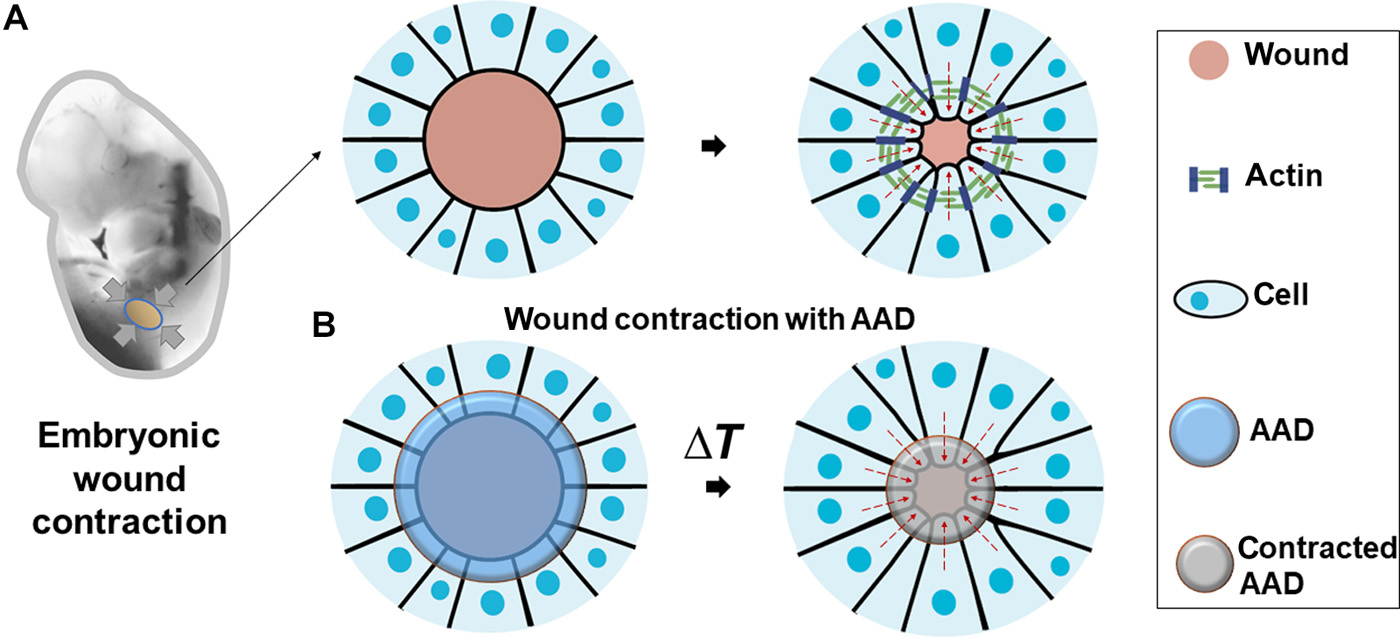
Fig. 1 Bioinspired design of AAD for promoting wound contraction.
当应用于伤口时,水凝胶与皮肤强烈结合。此外,人体热量加热PNIPAm,导致凝胶收缩。粘附的下层皮肤与其收缩,快速有效地使伤口愈合。同时,大多数可能引起感染的细菌被银纳米粒子杀死。
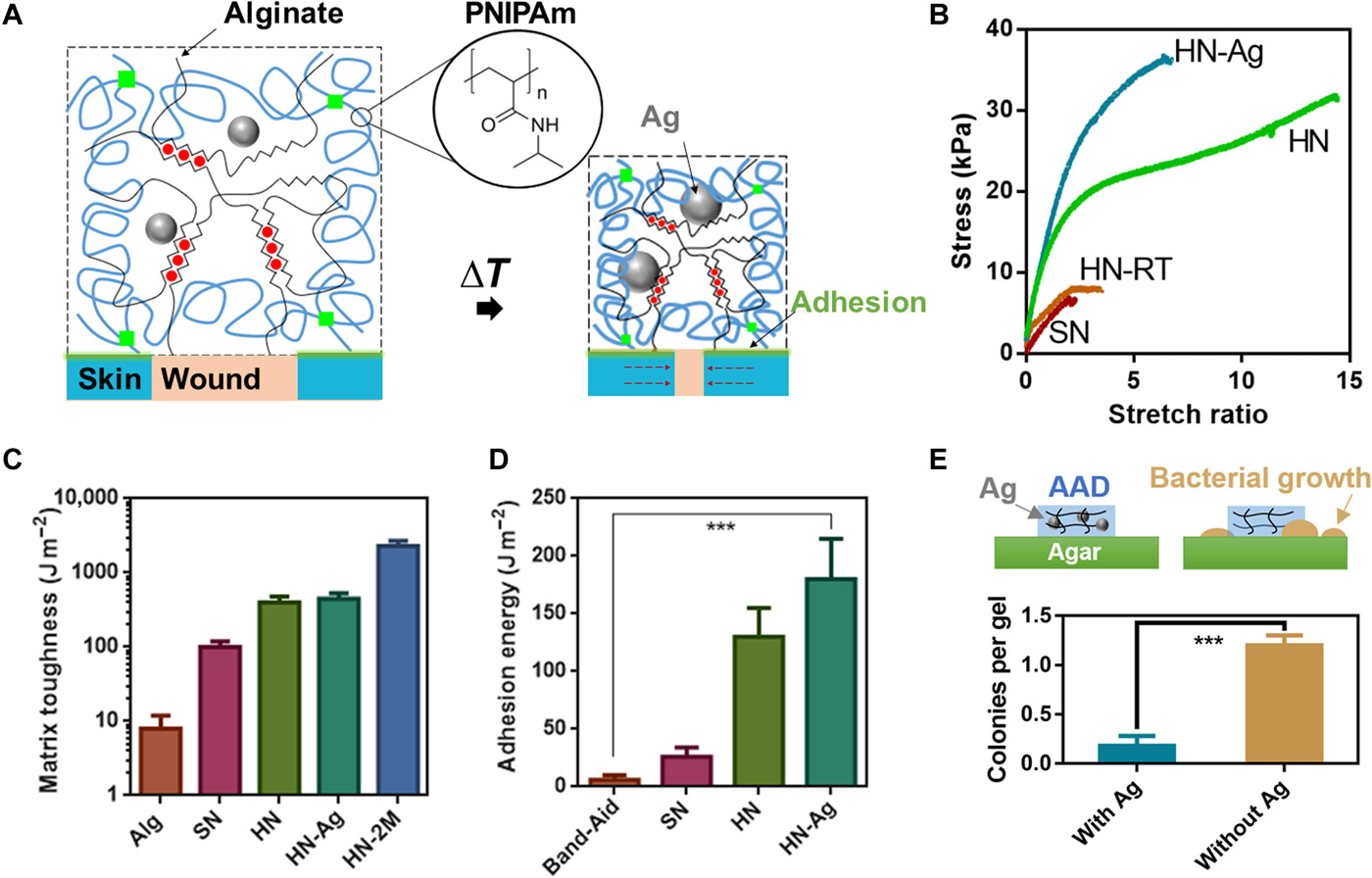
Fig. 2 Mechanical and antibacterial properties of AAD.

Fig. 3 Thermoresponsiveness of AAD and in vitro contraction on skin.
通过改变凝胶中PNIPAm的量,可以调节它将皮肤拉到一起的程度。这种控制可以派上用场,因为肘关节等关节上的皮肤需要在愈合时保持更大的伸缩性和柔韧性,而不是身体较平坦的部位。
在实验室测试中,研究人员发现AAD粘附在猪皮上的力量是创可贴的10倍。它还使小鼠的伤口面积减少了约45%,而对照组未经治疗的伤口在同一时期几乎没有减少。此外,它比其他测试的实验性愈合水凝胶能更快地使伤口愈合,并且它不产生炎症或免疫反应。
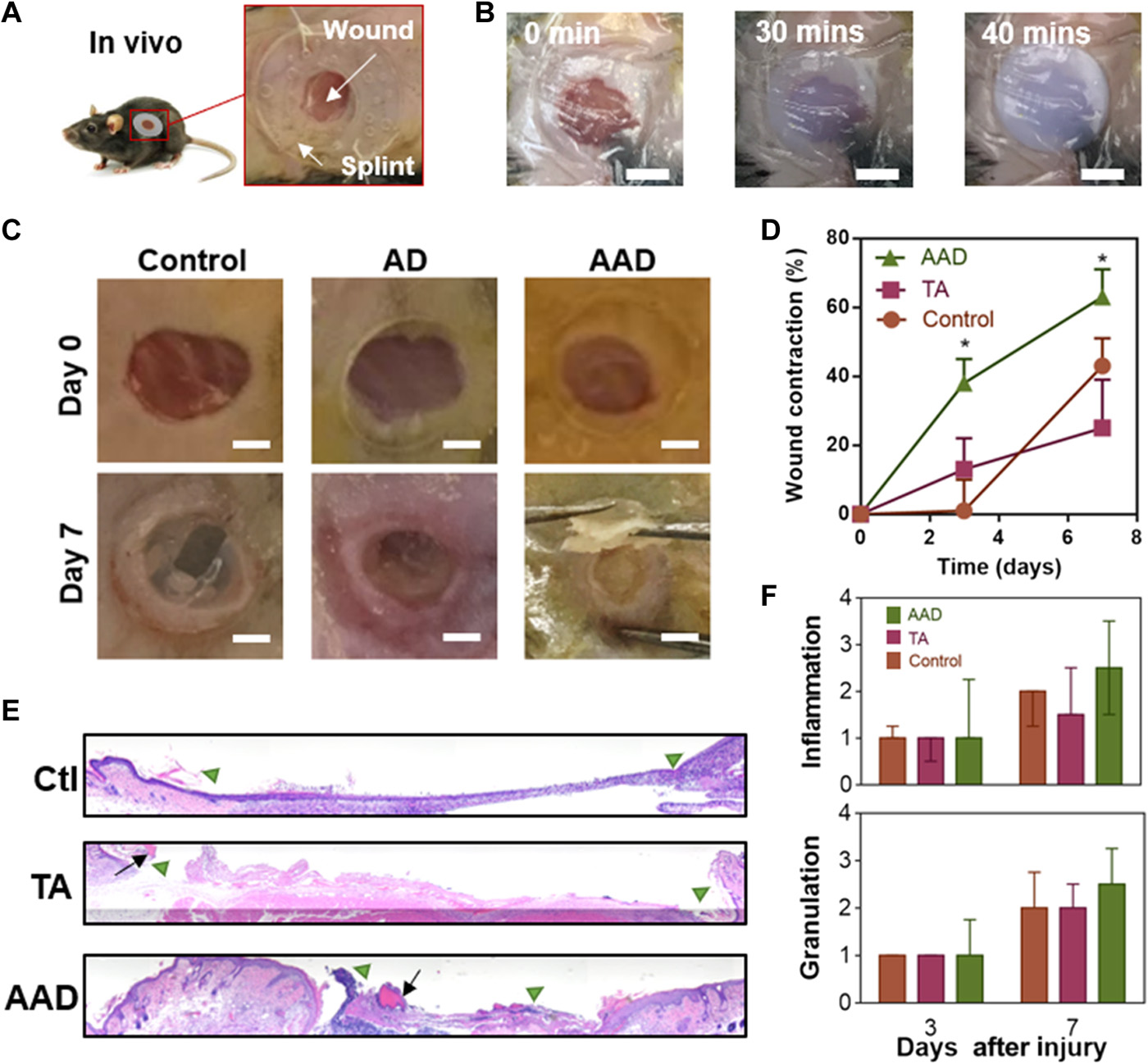
Fig. 4 In vivo wound healing with application of AAD.
“我们正在通过研究继续这项研究,以更多地了解AAD所施加的机械提示如何影响伤口愈合的生物学过程,以及AAD如何在不同温度范围内发挥作用,因为体温在不同位置会有所不同,”该项目的首席科学家、哈佛大学的Benjamin Freedman博士说道。“我们希望进行额外的临床前研究,以证明AAD作为医疗产品的潜力,然后努力实现商业化。”
关于这项研究的论文最近发表在《科学进展》(Science Advances)杂志上。
论文链接:https://advances.sciencemag.org/content/5/7/eaaw3963
下载:加速伤口闭合
- 天大崔春燕/刘文广、清华李舟 Sci. Adv.:抗溶胀生物降解水凝胶重塑电微环境驱动脑缺损后内源性神经再生 2026-05-30
- 四川大学王云兵/胡成团队 AFM:基于手性活性多肽交联的多功能水凝胶协同缓解氧化应激与纤维化重塑 - 实现心肌梗死精准治疗 2026-05-30
- 南通大学孙文旭/张雷团队 AFM:仿生界面工程设计兼具高拉伸与高灵敏度的双纳米复合水凝胶 2026-05-29
- 东华大学陈志钢教授团队 AFM:钙离子输送的自泵式Janus膜用于糖尿病伤口愈合 2026-04-26
- 陕科大王学川/党旭岗、温州医科大郑漫辉 AFM:可注射自修复生物质基水凝胶生物粘合剂用于伤口愈合和可穿戴生物电子一体化 2026-01-30
- 西安交大郭保林教授团队 Adv. Mater.:自适应伤口敷料用于伤口愈合与修复 2025-12-25
- 石河子大学贾鑫/孙美州团队 Matter:光热响应微针纳米酶构建植物-材料生物界面 - 实现精准养分递送与氧化应激调控 2026-03-16
