皮肤伤口在愈合过程中很容易受到外界细菌的感染,一旦发生感染将严重影响伤口愈合的进程。因此,作为一个理想的外用伤口敷料,除了能够加快伤口愈合之外,还应该具备抗菌和抗感染的性能。在众多的外用伤口敷料中,水凝胶敷料不仅能够维持创面的湿度、提供气体的置换,而且可以有效地吸收创面的分泌物,故受到了越来越多研究者的关注。然而,水凝胶本身一般不具有抗菌性能,需要外加抗生素或者抗菌剂来抑制细菌的感染。
目前,革兰阳性菌,特别是金黄色葡萄球菌(S. aureus),是造成伤口感染的最主要原因。替考拉宁(TPN)是一种万古霉素族糖肽类抗生素,对革兰阳性菌(包括耐药性的金黄色葡萄球菌)具有优异的抗菌性能。相比于万古霉素,TPN的抗菌活性更强而且毒副作用更小。不同于不被鼓励用于防治细菌感染的万古霉素,TPN在临床上常被用于皮肤和软组织感染、骨髓炎等的预防和治疗。
可注射的热致水凝胶在低温(常温)下以溶液状态存在,可以被注射,并且具有易与药物、细胞混合的特性;该类水凝胶注射到人体后,在体温下可自发物理凝胶化,将药物、细胞等物质原位包裹,其已被广泛应用于药物缓释和组织工程等领域。其中,热致凝胶化的PLGA-PEG-PLGA三嵌段共聚物是研究最为广泛的热致水凝胶,但其也面临实际能够成胶的聚合物分子量窗口较窄的不足。
在前期的工作中,复旦大学高分子科学系俞麟教授和丁建东教授发展了物理混合法拓展了PLGA-PEG-PLGA三嵌段共聚物成胶的分子量窗口。如图1所示,两种具有不同PEG/PLGA摩尔比的PLGA-PEG-PLGA三嵌段共聚物被合成,Copolymer A不溶于水,而Copolymer B易溶于水,两种聚合物均不能单独形成热致水凝胶;有趣的是,将这两种共聚物通过一定比例混合后即可得到可注射的热致水凝胶。
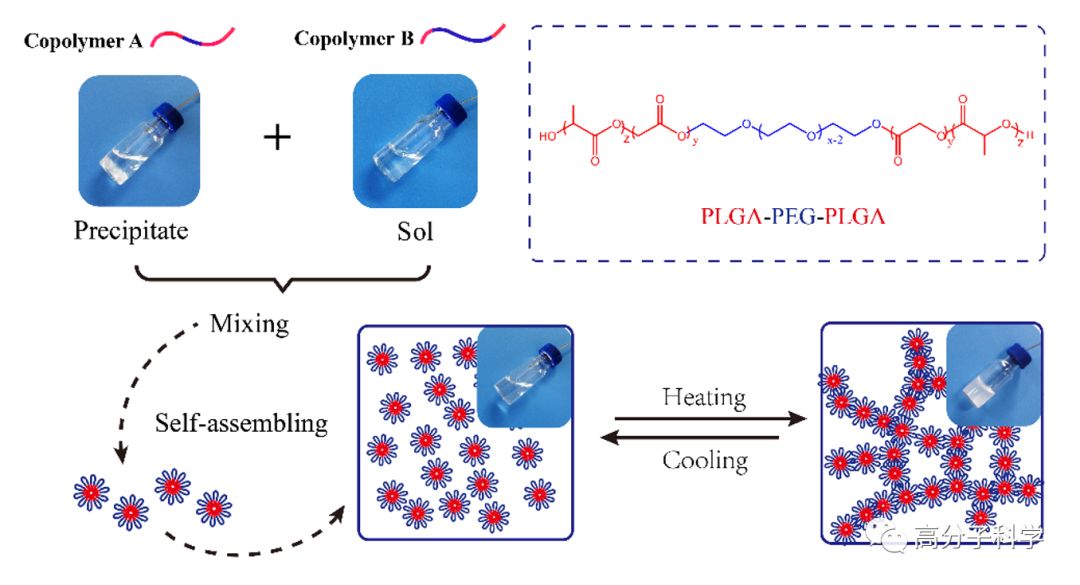
图1. 物理混合法制备热致水凝胶的示意图:将不溶于水的Copolymer A和易溶于水的Copolymer B混合后,由于合适的亲疏水平衡,聚合物混合物在水中能够自组装形成胶束,随着升温胶束能够聚集形成具有“逾渗胶束网络”的物理水凝胶
作者通过上述混合物热致水凝胶包载TPN尝试用于促进大鼠全切层伤口的愈合。体外释放实验表明TPN能够从水凝胶敷料中缓慢释放出来,释放周期超过3周;体外抑菌实验显示释放的TPN能够持续抑制S. aureus的生长。在大鼠全切层伤口模型中,载有TPN药物的聚合物混合物溶液可以在室温下方便地注射到伤口床中,由于大鼠的体温作用其能够在伤口床原位形成凝胶,方便地实现创面的覆盖(图2)。宏观的观测和病理学检测显示载药凝胶辅料的使用减少了创面的炎症反应,促进了胶原的沉积,加速了血管化,从而加快了伤口的愈合。由于PLGA-PEG-PLGA热致水凝胶的降解产物包括乳酸和乳酸盐,而这两者能够刺激血管化,促进成纤维细胞的增殖和迁移,同时降解产生的酸性环境也利于抑制细菌的生长,故作者认为PLGA-PEG-PLGA热致水凝胶辅料本身的特性结合TPN的抗菌活性共同加速了伤口的愈合。
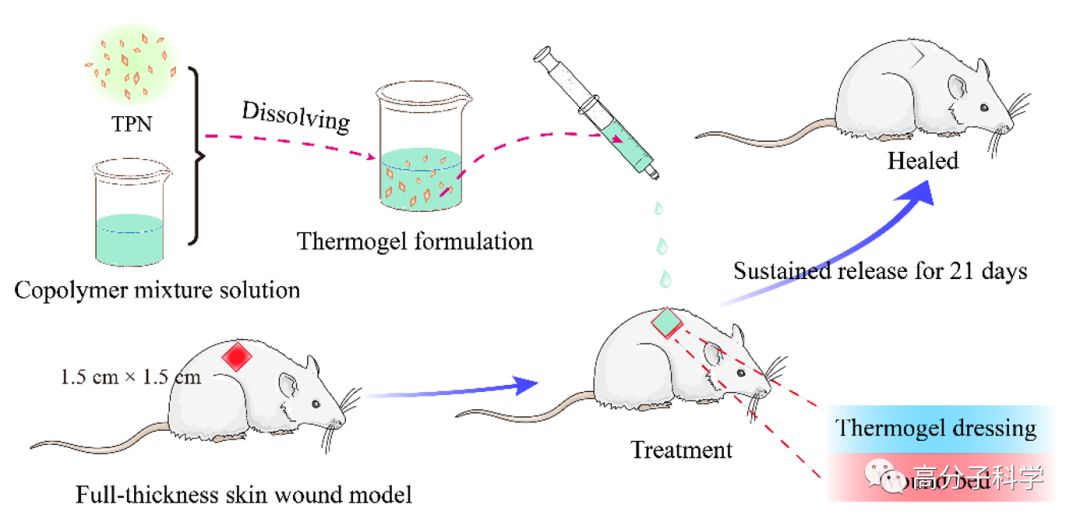
图2. 载药热致水凝胶敷料用于伤口愈合的示意图
徐维棵硕士研究生是该论文的第一作者,俞麟教授为该论文的通讯作者,复旦大学丁建东教授和重庆大学蔡开勇教授、刘鹏副教授为该论文的共同作者。该项工作得到了国家自然科学基金(51773043, 81772363,和21474019)、科技部重点研发计划(2016YFC1100300)以及中国博后科学基金(2018M632020)的资助。
该工作即将发表于Chinese Journal of Polymer Science。
论文链接:https://link.springer.com/article/10.1007/s10118-019-2212-5
- 复旦丁建东教授课题组《Adv. Funct. Mater.》:基于热致水凝胶的研究发明治疗/预防一体式肿瘤疫苗 2022-09-14
- 复旦大学俞麟教授和上海第十人民医院彭琛副研究员合作开发三模式生物成像技术用于揭示PLGA-PEG-PLGA热致水凝胶体内降解机理 2020-07-07
- 复旦大学丁建东教授课题组揭示热致水凝胶的微观结构与普适机制 2019-05-20
- 东华大学陈志钢教授团队 AFM:钙离子输送的自泵式Janus膜用于糖尿病伤口愈合 2026-04-26
- 陕科大王学川/党旭岗、温州医科大郑漫辉 AFM:可注射自修复生物质基水凝胶生物粘合剂用于伤口愈合和可穿戴生物电子一体化 2026-01-30
- 西安交大郭保林教授团队 Adv. Mater.:自适应伤口敷料用于伤口愈合与修复 2025-12-25
- 空军军医大学牛丽娜教授团队 ACHM:仿生结构协同免疫调控的DNA-胶原敷料实现烧伤无瘢痕再生? 2025-08-19
