点评 | 陈学思院士(中国科学院长春应用化学所)
药物载体的递送瓶颈与系统性清除
临床药物研发常面临药物系统毒性高、稳定性不足、靶向性有限以及生物利用度低等多重药理学挑战。递送载体通过实现药物的高效封装、稳定保护与靶向递送,有效破解上述难题,已成为当今生物医药领域的核心工具。近年来,高分子递送材料(尤其是具备出色生物互作特性的材料,如PEG、PLGA)已在临床普及应用,显著推动了肿瘤靶向化疗、mRNA疫苗、siRNA疗法及基因递送等多种前沿治疗策略的转化。然而,药物载体经静脉注射后普遍面临严重的非选择性系统清除问题,导致实际到达靶组织的有效剂量极低,严重限制了治疗效果。尽管已知肝脏单核吞噬系统是介导该过程的主要细胞群体,但当前领域既缺乏安全且具有普适性的干预策略,也尚未建立能够系统解释其高效清除行为的机制框架。相关研究长期停留在现象描述但机制缺失的状态,难以进一步实现实质性突破。
北京时间2026年3月20日,中国科学技术大学王育才团队在Science发表题为“Commensal-driven serotonin production modulates in vivo delivery of synthetic and viral vectors”的研究论文。汪沁、陈子琦和张国荣博士为文章共同第一作者,王育才、朱书和蒋为教授为本研究的通讯作者。
研究团队通过系统的多器官偶联活体显微成像和多平台递送体系验证:药物递送过程本质上是材料与机体生理系统相互作用的结果,限制其递送效率的关键环节来源于多器官之间的动态调控,而非仅仅单一材料参数的优化;通过干预新发现的递送调控机制,可以广谱性提升各类高分子载体材料的终端递送效率与疗效。这一认识将递送问题从传统“材料优化”范式提升至“系统调控”层面,为后续高分子载体材料的理性设计提供了新的理论指导框架。
文章简介
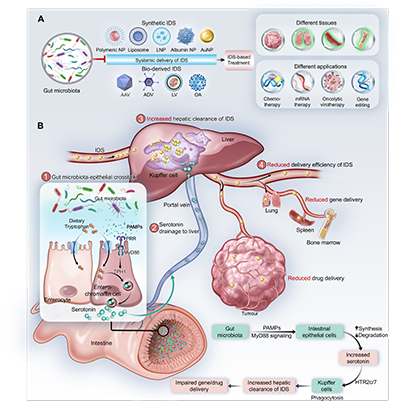
机体清除药物递送载体的底层机制与调控策略
该研究揭示了一条由肠道共生菌驱动、肝脏执行的药物载体清除机制,该机制刺激并维持机体对外源载体材料的清除能力,使静脉注射的高分子载体非选择性地大量聚集于肝脏,导致药物快速失活、降解、排泄。这种肝脏与病变组织竞争药物摄取的行为,正是当前载体药物临床疗效远低于预期的重要原因。
团队在肿瘤模型和基因编辑模型中,充分验证了该机制对于提升高分子载体递送效率的指导意义。通过靶向干预该机制中核心环节,可显著抑制肝脏对高分子载体的非特异性清除,从而在不改变材料本身特性的前提下,实现递送效率和治疗疗效的稳定提升。本研究通过调控非靶器官功能,重塑靶器官对递送载体的摄取效率,进而系统性提升整体递送效能,推动递送调控研究从单一器官的局部调控模式,向多器官协同的整体调控模式实现跨越。
总体而言,团队证实了团队证实了该清除调控机制作为跨器官网络的关键节点,对高分子载体递送效率具有决定性的核心作用。该研究不仅揭示了影响递送效率的关键系统性机制,也重塑了材料领域对体内递送问题的基本认知边界,为精准肿瘤治疗与基因治疗等依赖高效体内递送的前沿技术提供了新的解决路径。
核心数据简介
团队发现,清除小鼠肠道共生菌可显著提升多类载体向肿瘤组织的递送效率,包括聚合物纳米颗粒、脂质纳米颗粒(LNP)、脂质体、白蛋白纳米颗粒(图1),并且这种递送效率的提升可直接转化为多种抗肿瘤治疗策略的疗效增强。例如,联合肠道菌清除与纳米化疗药物处理,可显著提高晚期结肠癌、晚期乳腺癌、晚期黑色素瘤小鼠对化疗的响应性;相比之下,单独应用纳米化疗药物仅在早期阶段抑制肿瘤生长,对生存获益有限。通过对多模型、多载体、多药物的分析,肠道共生菌清除可将各类化疗药物的抗肿瘤疗效提升5倍以上。除肿瘤治疗外,肠道菌清除可显著增强高分子载体介导的多器官体细胞基因编辑效率,并提高基于mRNA的蛋白替代疗法的治疗效果,进一步支持该调控机制在不同技术体系中的广泛适用性。药代动力学分析表明,肠道菌清除能够显著延长多类载体的体内循环时间,从而系统性提高其终端递送效率。这些结果表明,肠道共生菌在生理稳态下对载体的体内递送具有普遍性的抑制作用。
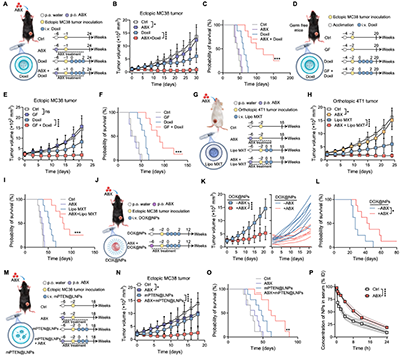
图1、肠道共生菌缺失可广谱性提高各类载体的血液循环能力,从而显著增强载体的系统性递送效率与相关疗法的疗效。
为解析肠道共生菌调控载体体内循环的机制,团队开发了一套基于活体成像的单细胞形态及载体定量分析系统,实现了在活体水平对载体与细胞之间动态互作过程的实时追踪(图2)。基于该分析平台,团队构建了肝脏吞噬细胞在不同生理状态下的行为与形态学全景图谱,定量揭示了肠道共生菌对肝脏吞噬细胞功能状态的调控作用,发现肠道菌清除可显著抑制肝脏吞噬细胞对各类载体的摄取能力(下降幅度最高可达70%),并诱导其发生显著的形态学重塑和表型转变。以上结果表明,肝脏吞噬细胞的稳态吞噬功能依赖于肠道菌的持续调节。
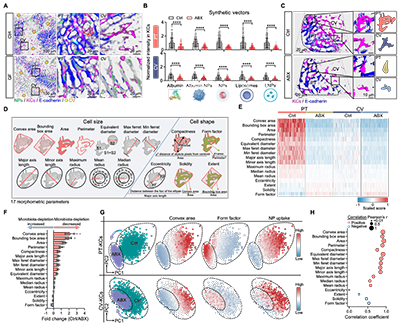
图2、使用活体成像研究高分子载体的体内转运与生物互作过程。
进一步的,一条完整的肠—肝—递送调控轴得到了系统解析:肠道共生菌持续激活肠道上皮内分泌系统,促进并维持血清素的产生与分泌;血清素作用于肝脏吞噬细胞,维持其稳态活化状态并增强其对载体的吞噬能力;在器官水平,肝脏吞噬细胞介导了肝脏对载体的高效非选择性清除,从而降低其体内循环能力并限制其向靶组织的有效递送。这一跨器官调控轴从机制上揭示了载体“非特异性清除”现象的生物学基础,将其从经验性观察上升为可被系统解析与调控的内在过程,并为突破递送效率瓶颈提供了明确的干预靶点与理论依据。
在应用层面,针对血清素信号轴的干预为提升体内递送效率提供了一种无需改造材料本身的普适性策略。无论是通过药理学手段阻断血清素刺激信号,还是通过饮食限制其前体色氨酸的摄入,均可有效抑制肝脏吞噬细胞介导的非特异性清除,从而系统性延长载体循环时间并增强其靶向递送能力,在多种治疗模型中实现显著的疗效提升(图3)。
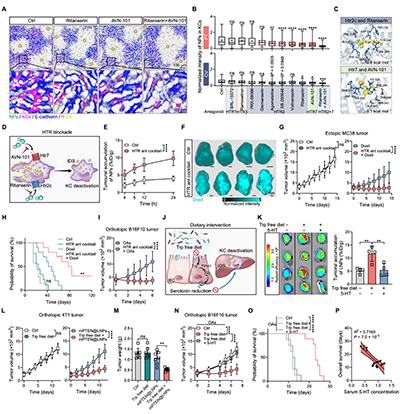
图3、靶向干预血清素信号轴可显著增强各类载体的系统性递送效率与相关疗法的疗效。
相关成果在线发表在Science 391, eadu7686 (2026). DOI: 10.1126/science.adu7686。
【点评】陈学思院士(中国科学院长春应用化学所):
长期以来,高分子药物递送材料以“材料属性驱动”为核心路线,研究者通过调控材料结构、组成及组装行为优化载体性能,这一思路在以聚乳酸及其衍生体系为代表的可降解高分子材料研究中成效显著,为递送技术发展奠定了基础。为进一步提升体内递送效率,除了持续进行材料结构的优化,还应关注材料设计与体内行为之间的关联。尤其是在复杂生理环境中,递送材料需跨越多层级复杂的生理屏障,导致单一材料参数与最终递送效率之间往往缺乏稳定且可预测的内在关系,成为制约高分子等递送体系进一步发展的关键科学问题。
该项工作的重要意义,在于从非材料优化视角拓展了设计逻辑:载体体内行为是材料与生理系统动态作用的结果,而非材料属性单向决定。作者证实,载体清除与分布受跨器官调控网络影响,可通过调控非靶器官改变载体体内命运,这一发现拓展了设计空间,使材料设计升级为结构与体内环境协同调控的综合策略。从临床应用需求来看,未来高分子递送材料设计,既要坚守结构、降解性等核心基础,也要考虑材料在生理环境中的动态响应及与多器官的耦合关系,其性能由结构与环境共同塑造。这一理念转变将推动递送材料从“结构导向”走向“系统导向”,促进材料科学与生命科学跨学科协同,突破技术瓶颈。
总体而言,该工作深化了对递送过程的认知,普适性地将传统材料的递送能力提升到更高水平,为高分子材料在核酸药物、精准治疗中的应用提供了新路径,对领域高质量发展具有引领作用。
论文链接:https://www.science.org/doi/10.1126/science.adu7686
- 浙江大学王立教授、俞豪杰教授团队 JCIS:用于安全磁共振成像和刺激响应药物递送的纳米粒子 2025-09-09
- 东南大学葛丽芹教授与合作者 Research:微气泡为模板的免疫活性金属多酚胶囊用于药物递送和增强的肿瘤免疫治疗 2025-07-31
- 四川大学丁明明教授团队 Angew: 可视化β折叠到β转角构象转变的荧光聚合物囊泡及其用于颜色报告型药物递送 2025-07-11
- 大连理工大学王忠刚教授课题组在抗肿瘤纳米药物高分子载体研究领域取得进展 2019-11-22
- 复旦大学陆伟跃教授团队与药物制剂国家工程研究中心王浩研究员联合研制了一种肿瘤微环境响应型控制药物释放的硼替佐咪纳米药物制剂 2019-03-18
- 华东师范大学程义云教授在含氟高分子载体最新研究进展 2018-04-18
