植入3D 打印支架是治疗骨缺损的有效方法之一。然而,骨骼修复的过程极其复杂,涉及炎症阶段、修复阶段和重塑阶段,每个阶段都需要一系列生物活性分子的协调控制。因此,理想的骨修复支架应能够根据骨组织愈合过程释放不同生物活性分子。近日,暨南大学罗丙红教授团队联合中国科学院深圳先进技术研究院的赖毓霄研究员团队共同开发了一种具有多种药物和活性分子分时控释的多功能3D打印促骨再生支架。

该团队通过聚多巴胺(PDA)成功地将天然抗菌剂—丁香酚和载有成血管的二甲基草酰甘氨酸(DMOG)的层状双氢氧化物(LDHs)加载到 3D 打印的 PLLA 支架表面(图1)。由于丁香酚的早期释放,支架最初表现出很强的抗菌作用,而 LDH 持续释放的 DMOG 在后期提供了促进长期的成骨和血管生成的能力。此外,负载DMOG的LDH进行表面改性有效地增强了 3D 打印 PLLA 支架的机械性能。重要的是,LDH的存在还通过释放 Mg2+赋予了支架优异的成骨活性,可与 DMOG 和丁香酚协同作用,刺激血管生成和成骨分化。分时控释的活性支架有望成为骨组织工程支架非常有效的构建方法。

图1. 利用 DMOG 和丁香酚的时空控释并协同离子效应构建多功能 3D 打印 PLLA 复合支架示意图
在这一研究中,该团队利用PDA将负载DMOG的LDHs(LDHsD)和丁香酚(Eug)同步修饰到3D打印的PLLA支架表面。由于PDA与LDH含有丰富的氨基和羟基,因此修饰后的复合支架亲水性增强。此外,LDH也在一定程度上提高了PLLA支架的力学性能,数据表明在湿态下,复合支架的压缩模量和强度分别比纯PLLA支架高11.4%和 7.9%(图2)。亲水性的改善与力学性能的增强均有利于促进细胞的粘附和铺展,从而提高支架材料的细胞亲和性。

图2. 支架的理化性能表征
体外药物释放实验显示了丁香酚的早期快速释放,以及DMOG和Mg2+的长期持续释放的结果,这也印证了体外抗菌实验中添加有丁香酚的复合支架对金黄色葡萄球菌和大肠杆菌的24小时抑菌率均达到85%以上。与此同时,体外细胞实验也显示了复合支架优异的生物相容性和细胞亲和性(图3)。

图3. 支架的体外抗菌活性、细胞毒性与细胞粘附性能
通过体外成骨与成血管化实验的深入验证,该研究证实了LDHs、DMOG与丁香酚协同促进了成骨基因与成血管基因的上调,从而表现出支架的钙结节生成能力的提高以及细胞迁移能力与小管形成性能的改善(图4)。此外,通过体内大鼠颅骨临界性缺损动物模型发现复合支架组的骨体积分数(BV/TV)和体积骨密度 (BMD) 均显著高于 BLANK 组和 PLLA 组,由此也进一步验证了复合支架优异的促进骨生成的能力(图5)。
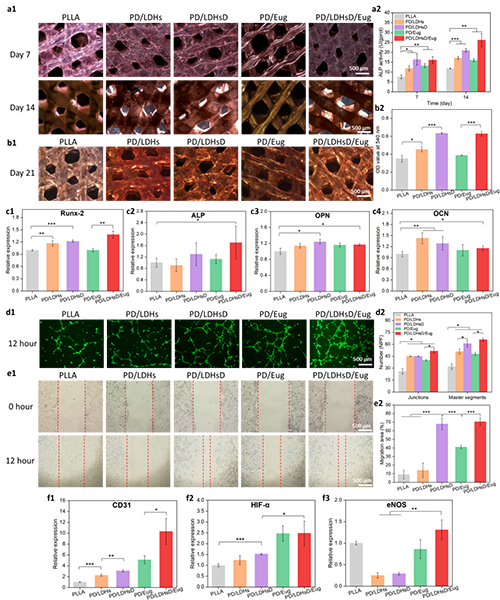
图4. 支架的体外成骨成血管化实验表征
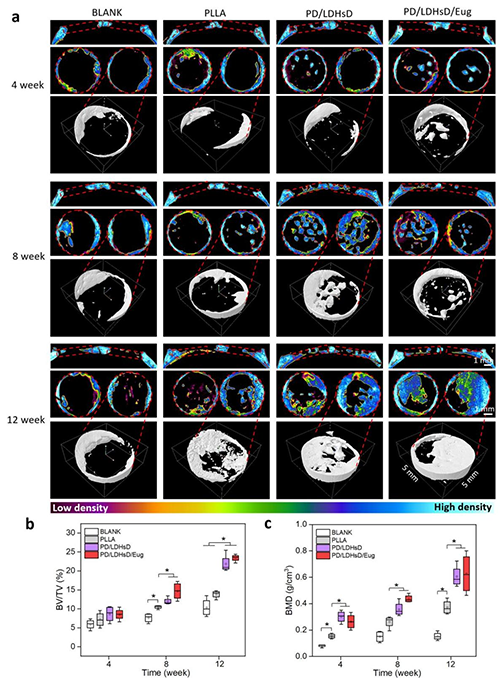
图5. Micro-CT分析评估植入支架修复大鼠临界性颅骨缺损效果
相关工作以“Versatile 3D Printing Scaffold with Spatiotemporal Release of Multiple Drugs for Bone Regeneration”为题发表在《ACS Nano》(doi:10.1021/acsnano.4c13265)上,暨南大学化学与材料学院罗丙红教授与中国科学院深圳先进技术研究院的赖毓霄研究员为论文共同通讯作者,暨南大学化学与材料学院2020级研究生朱泽林与中国科学院深圳先进技术研究院的副研究员李彩荣为论文的共同第一作者。该研究得到国家自然科学基金、广东省自然科学基金和重点研发计划等多方支持。
原文链接:https://doi.org/10.1021/acsnano.4c13265
- 西工大黄维团队官操教授 AM:数字化制备三维液态金属水凝胶 2026-05-28
- 中国科大/伍伦贡大学 AFM 封面:基于面投影光固化技术的仿生梯度抗冲击结构材料 2026-04-17
- 南林刘承果教授团队 Adv. Sci.:用于3D打印的高性能、可循环生物基光敏聚合物 2026-03-28
