不可触及的皮下实体瘤,尤其是深部乳腺癌和黑色素瘤,已成为最常见的恶性肿瘤之一,对人类健康构成严重威胁。局部精准治疗对于皮下肿瘤的治疗意义和有效性日益受到重视,这归功于其与传统全身化疗相比具有无可比拟的优势,包括可忽略的系统毒性、疗效稳定、操作微创等。这是一种对患者友好且安全的药物输送方法。在这种情况下,对肿瘤的透皮给药将提供长期有效的递送,并且该方法可用于癌症治疗中的局部免疫激活和后续精准反复治疗。其中,微针贴片通过局部递送抗肿瘤药物,如姜黄素、阿霉素和癌症疫苗等,已被证明其在肿瘤治疗中的巨大应用潜力。微针可以无痛地穿透皮肤,克服角质层屏障,并创建微通道以增强药物输送。此外,微针贴片还可以联合物理治疗(例如热疗),即进一步利用物理治疗的破坏力摧毁肿瘤组织上的相互作用结构并加速癌细胞凋亡,从而增强协同治疗,同时使响应性治疗成为可能。然而,现有微针贴片仍面临易从皮肤表面脱落、药物暴露时间短等局限性。同时,微针通常依赖于被动扩散,这限制了治疗有效负载药物的穿透深度和分布。为了解决这些挑战并提高药物输送效率和持续时间,采用不同的工程化设计策略增强微针递送药物透过表皮到达深层组织的渗透具有重要意义。
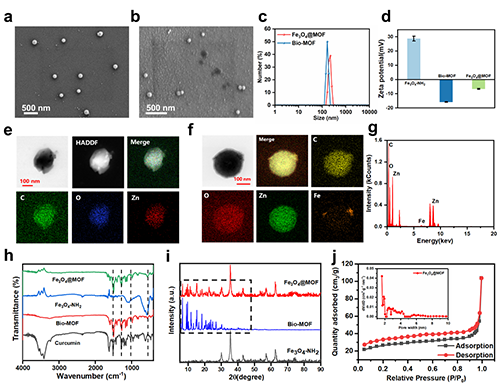
图1 磁性生物金属有机框架的制备与表征
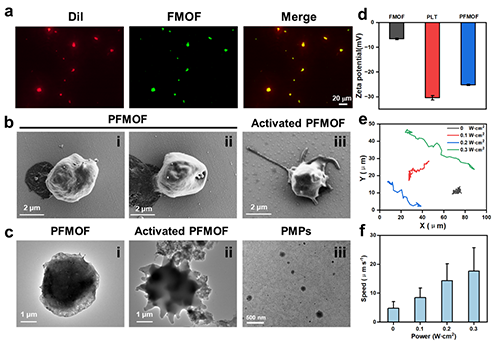
图2 工程化血小板的制备与表征
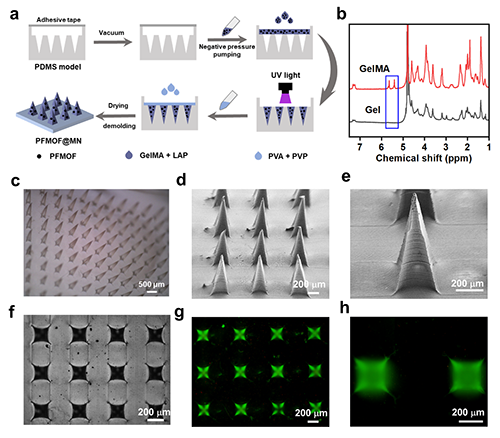
图3 工程化血小板集成可分离微针贴片的构建与表征
该研究论文以“ Microwave-Responsive Engineered Platelet Microneedle Patch for Deep Tumor Penetration and Precision Therapy”为题于2025年2月在《ACS Applied Materials & Interfaces》上发表,东南大学硕士生刘宗浩为第一作者,葛丽芹教授为该论文通讯作者。
原文链接: Zonghao Liu, Fangzhou Liu, Diyi Feng, Weikun Li, Xin Tan, Ning Yang, Yanling Liang, Nuoya Chen, Qiang Cheng, Liqin Ge. Microwave-Responsive Engineered Platelet Microneedle Patch for Deep Tumor Penetration and Precision Therapy. ACS Appl. Mater. Interfaces. 2025. 17, 10457-10469.
DOI: 10.1021/acsami.4c20896
https://pubs.acs.org/doi/full/10.1021/acsami.4c20896
- 东南大学葛丽芹教授/刘玲教授 CEJ:多功能微针贴片与电刺激协同调节伤口微环境 促进感染糖尿病伤口愈合 2025-02-17
- 康复大学周祺惠团队/青大附院王志国 AFM:生物活性角蛋白水凝胶微针贴片用于病理性瘢痕治疗 2024-10-03
- 康复大学周祺惠/易兵成 J. Adv. Res.:模拟蚊喙无感知叮咬机理开发出凹面微针贴片用于眼部麻醉 2024-08-24
- 中国药科大学孙敏捷教授团队:ATP超敏型蛋白团簇用于肿瘤深层渗透及放大MRI引导的光热治疗 2019-08-06
- 四川大学王云兵/胡成团队 AFM:基于手性活性多肽交联的多功能水凝胶协同缓解氧化应激与纤维化重塑 - 实现心肌梗死精准治疗 2026-05-30
- 港中大(深圳)唐本忠院士团队 ACS Nano:可注射NIR-II水凝胶实现荧光成像引导的肥胖局部精准治疗 2026-05-24
- 澳门大学王瑞兵团队 JACS: 乏氧诱导的超分子自由基实现胞内聚合介导的肿瘤精准治疗 2025-01-15
