港大徐立之团队《Nat. Commun.》:基于超连接纳米纤维网络的高导电强韧水凝胶
2023-02-12 来源:高分子科技
水凝胶由于其良好的结构柔性、较高的通透性和出色的生物相容性,是构建软电子和生物医学设备的理想材料。近年来导电水凝胶的不断发展,为可植入生物电极、软体致动器、组织工程平台、太阳能水处理和其他先进技术创造了更多的可能性。然而,尽管进行了大量的研究工作,在水凝胶中同时实现高导电性和机械强韧性仍然具有挑战性,大大限制了它们的实际应用。传统导电水凝胶的制备中在聚合物基质中加入导电填料来赋予水凝胶导电性。然而,这些方法获得的导电水凝胶性能并不理想。一方面,为构建导电通路,提高导电性,往往需要加入大量的导电填料;另一方面,大量导电填充物的加入,通常伴随着水凝胶机械性能的下降,限制了其的应用场景。纯导电聚合物水凝胶的开发获得了高的电导率,但导电聚合物固有的脆性使这些水凝胶表现出较低的机械强度。
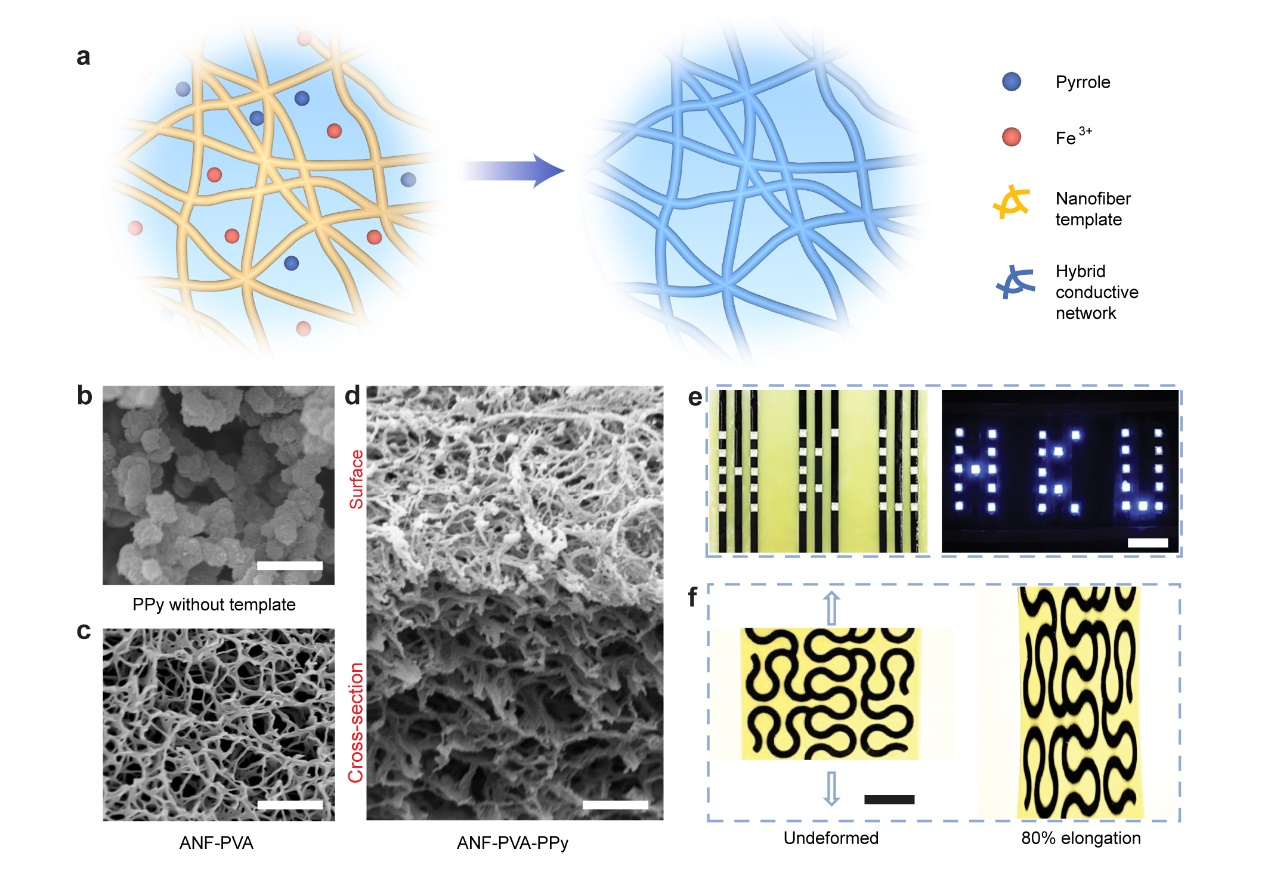
图1,CNHs的合成及结构表征

图2,CNHs的导电性
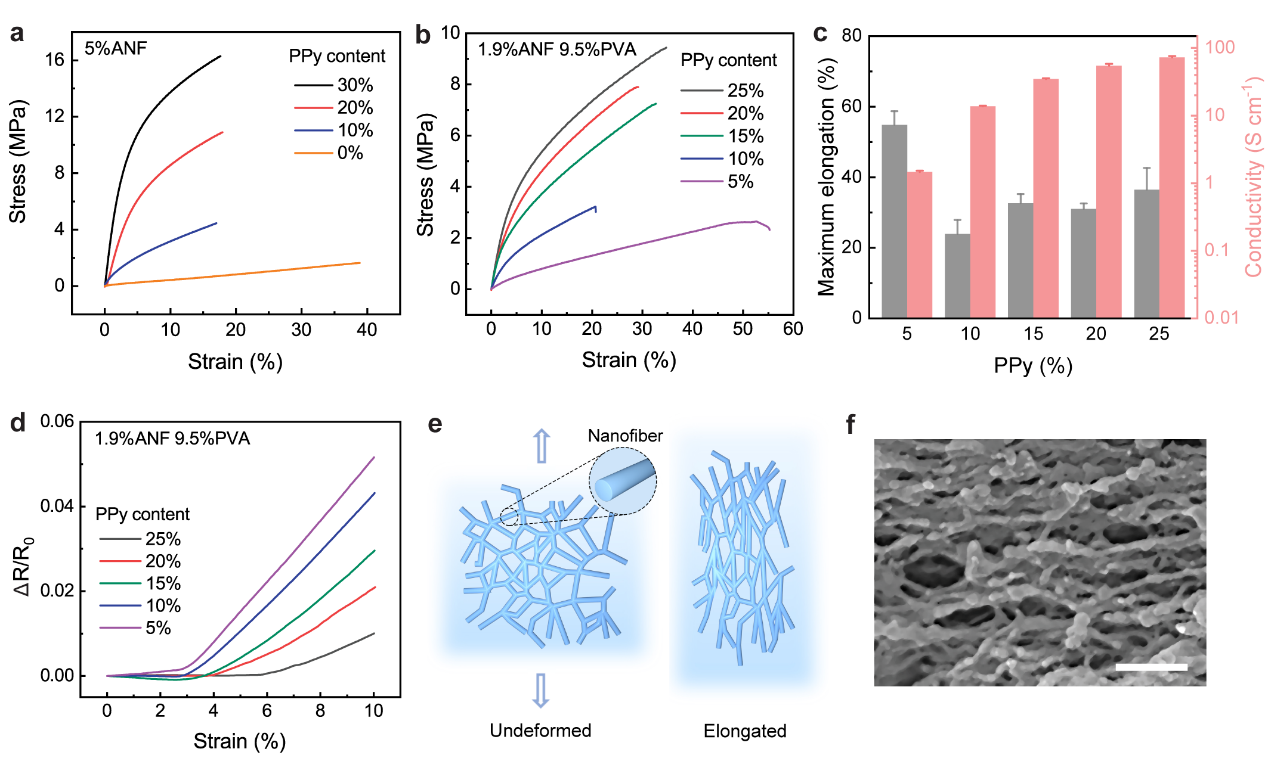
图3,CNHs的机械性能
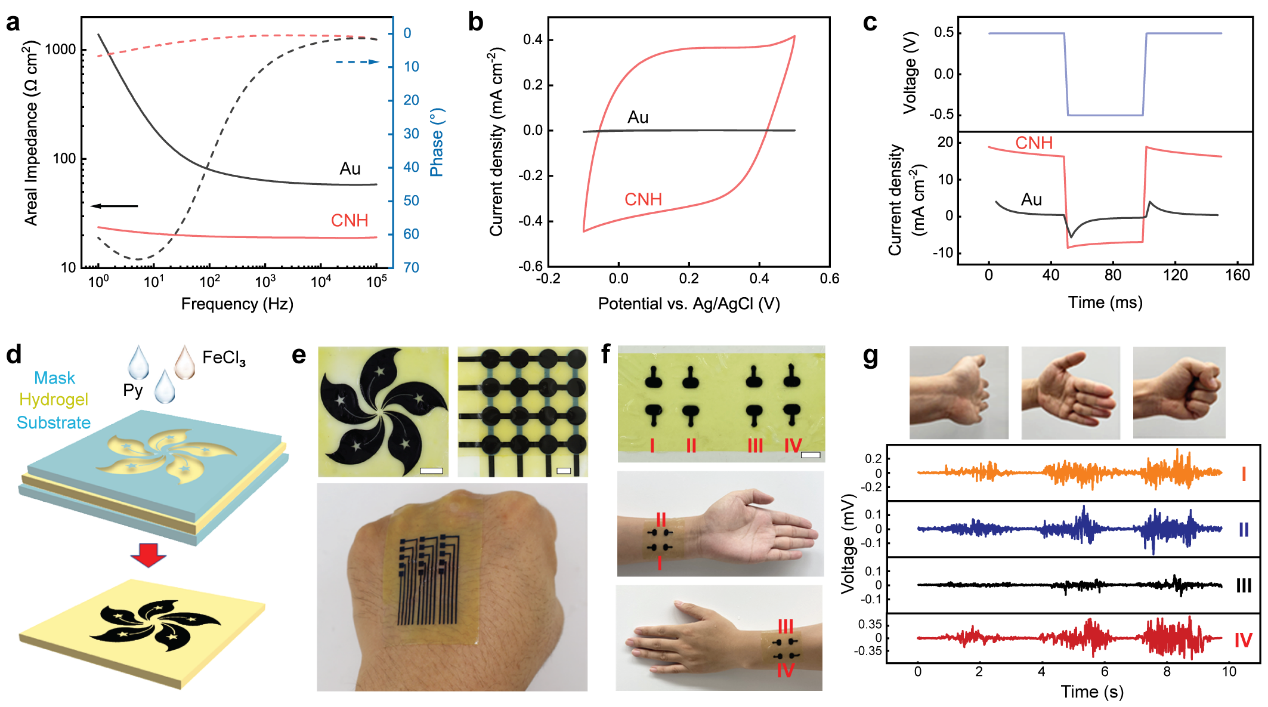
图4,CNHs在软生物电子学中的应用
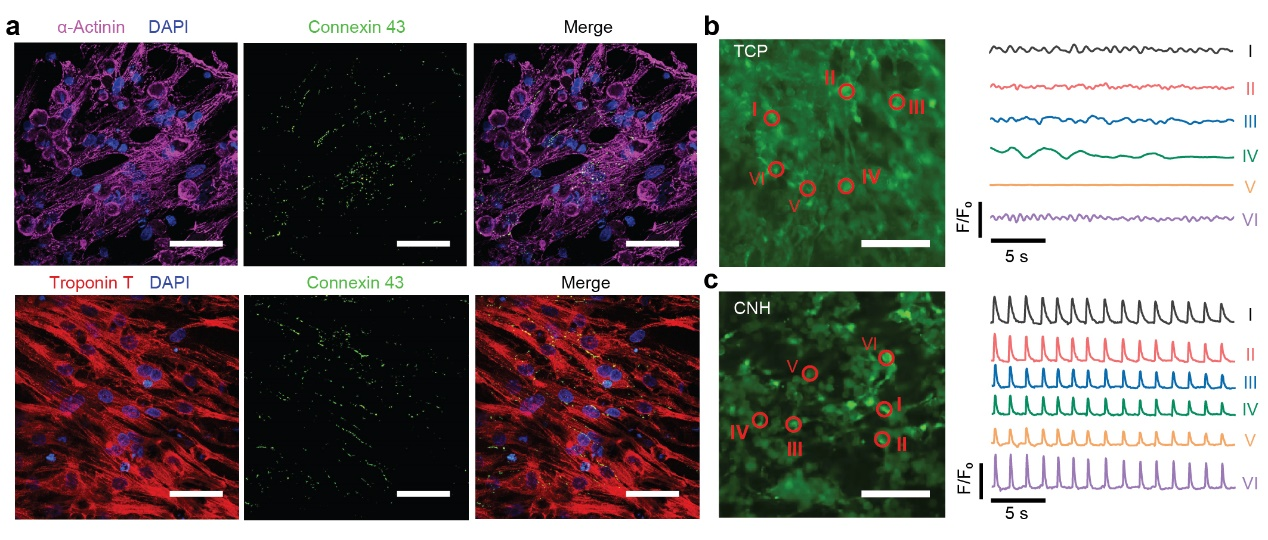
图5,CNHs用于调控心肌细胞
论文链接:https://www.nature.com/articles/s41467-023-36438-8
课题组主页:https://xulizhi.hku.hk
版权与免责声明:中国聚合物网原创文章。刊物或媒体如需转载,请联系邮箱:info@polymer.cn,并请注明出处。
(责任编辑:xu)
相关新闻
- 东华大学朱美芳/成艳华团队 Adv. Mater.:轻质热防护材料助力空间离轨与柔性舱展开系统 2026-06-02
- 中国科大龚兴龙教授团队《ACS Nano》:界面氢键增强的仿生芳纶纳米纤维网络 - 实现在极端环境下的多功能防护 2023-01-31
- 兰州大学王凯荣教授课题组 ACS Nano:一种由天然抗菌肽和ADP构建的多功能水凝胶 2022-05-14
- 上海交大张智涛团队 Adv. Mater.:面向表皮电子的新型高导电银浆生物粘合剂 2026-03-13
- 东南大学张久洋教授课题组 Adv. Mater.:基于无机硅网络界面交换的液态金属油墨 2025-06-20
- 无线植入设备实现脑肿瘤精准治疗 - 中山大学徐炳哲团队突破胶质瘤治疗难题 2024-12-15
- 麦吉尔大学李剑宇教授团队 Nature: 工程化强韧血凝块实现快速止血与组织再生 2026-04-30
