有机砷类小分子或无机砷类药物造福了全球无数的血液肿瘤患者,但将其用于实体肿瘤治疗的临床转化却成效甚微。全世界范围内的多起临床I/II试验表明,砷类药物对于乳腺癌、肝癌、结肠癌等10余种实体肿瘤并未展现出可观的疗效。其原因主要为砷类药物在血液循环时间短、易与蛋白质等结合造成毒性、肿瘤累积量低等,而加大其用量又会引起严重的毒副反应。作为一种新近报道的二维(2D)材料,砷烯由单元素砷(As0)组成,其毒性比传统砷类药物低,但对血液肿瘤细胞具有相似的优异治疗效果。考虑到实体肿瘤相对于正常组织具有较高的内源性H2O2,砷烯有望在肿瘤组织累积后可被选择性氧化为高毒性的氧化态,从而在实现肿瘤激活的特异性治疗的同时,降低全身毒性。此外,砷烯是一种具有间接带隙的半导体,其理论上具有近红外光响应的光热性能。因此,砷烯氧化程度越高,其对正常组织毒性越大,对肿瘤特异选择性越低,同时光热转换效率也越低。目前基于隔绝空气等复杂操作的砷烯液相超声剥离制备,所得到的砷烯尺寸大,不适用于生物应用,且过程仍易导致氧化。因此,为了增加砷烯用于产业化的可能性,需要探究在大气环境中制备高纯度砷烯的新方法,且砷烯的实体肿瘤治疗评测及生物安全性仍鲜有报道。
近期,哈佛大学医学院陶伟教授团队、杭州师范大学药学院谢恬教授与中科院宁波材料所吴爱国教授团队合作,结合课题组近期针对砷等元素的药物应用归纳(Chem. Soc. Rev., 2021, 50, 2260-2279)、前期对单元素二维材料在生物应用领域的总结(Chem. Soc. Rev., 2019, 48, 2891-2912)以及砷族元素在生物医学应用领域的系统性工作(Proc. Natl. Acad. Sci. U. S. A., 2020, 117(46): 28667-28677;Nat. Commun., 2020, 11(1): 2778;Nano Letters, 2020, 20(5): 3943-3955;Matter, 2020, 2(2): 297-322;Chem. Soc. Rev., 2019, 48(11): 2891-2912;Adv. Mater., 2018, 30(38): 1802061;Angew. Chem. Int. Ed., 2017, 56(39): 11896-11900;Adv. Mater., 2017, 29(1): 1603276;etc.),从材料学和生物学角度出发,提出利用单质砷烯作为新型砷类纳米药物对实体肿瘤进行高效治疗,拓展对砷类药物的认知。文中报道了砷烯具有(1)高生物安全性(高纯度单质砷固有毒性低),可从根本解决传统砷类药物固有高毒性的弊端;(2)肿瘤微环境激活的特异性及选择性的实体肿瘤化疗治疗效果(高纯度单质砷毒性低,但可被肿瘤微环境中过表达的H2O2等氧化为高毒性氧化态);(3)近红外光响应的肿瘤光热性能,将其从单一化疗药推向纳米光子药物;(4)与榄香烯(提取自中药的化学成分明确的抗癌药物,杭州师范大学谢恬教授为该药物的发现和推广者)联合可实现低剂量给药下的协调增效杀伤肿瘤效果。
作者从砷元素的存在形式及相应毒性分析出发,无机砷比有机砷的毒性大,三价砷比五价砷的毒性大,而单质砷具有较低毒性,主其要以灰砷(α-砷)、黑砷(β-砷)和黄砷(γ-砷)这三种同素异形体的形式存在。其中,灰砷有类似石墨的分层晶体结构,是由许多互锁竖起的六元环所构成的双层结构,层与层之间的结合力弱。作者基于灰砷的材料学结构特性,在N-甲基吡咯烷酮有机溶液和维生素C的引入条件下,通过超声破碎的液相剥离方式,制备出单质纯度高的、尺寸小(~3 nm)的砷烯纳米点(AsNDS)材料,并对其表面进一步的DSPE-PEG修饰(AsNDs@PEG)。维生素C可充当“保护剂”,防止大气环境制备过程中砷烯的氧化(图一)。

图一 (A)砷烯纳米点(AsNDs)的制备、表征及细胞选择性杀伤潜在机理。AsNDs的(B)透射电镜图像,(C)高分辨投射电镜图像,(D)AFM图像;AsNDs的(E)元素能谱图,(F)XRD图谱,(G)(H)XPS图谱,以及(I)拉曼图谱
随后,作者通过分析AsNDs@PEG对多种肿瘤细胞和正常细胞的毒性,发现其在一定浓度范围内可实现对肿瘤细胞的高效杀伤,而对正常细胞没有显著的毒性。通过AsNDs@PEG对细胞活性氧(ROS)、超氧化物歧化酶(SOD)、线粒体极化和膜形貌、DNA免疫荧光损伤、细胞周期分布、克隆形成能力、成瘤能力等方面的分析发现,AsNDs@PEG被肿瘤细胞吞噬后,更高程度地被H2O2等氧化,而氧化形成的高价态砷化合物对肿瘤细胞造成损伤(SOD酶活性下降、ROS清除能力下降、线粒体膜电位下降、DNA损伤、细胞周期阻滞、克隆形成能力减弱、细胞成瘤能力降低等)。
紧接着,作者比较了AsNDs@PEG和临床化疗药物(Dox)对皮下荷瘤小鼠的化疗能力。在同等剂量和给药次数下,AsNDs@PEG与Dox具有相媲美的化疗效果。5.0 mg kg-1的AsNDs@PEG(肿瘤抑制率67.9%)或5.0 mg kg-1的Dox(肿瘤抑制率74.6%)可以显著抑制肿瘤生长。此外,接受5.0 mg kg-1的AsNDs@PEG治疗的小鼠达到了25%的完全治愈率,而相比之下,接受相同剂量的Dox会造成明显的肝脏疾病、脾脏弥散性红髓扩张等损伤及心脏纤维化百分比增加、引起免疫系统损伤、体重及脏器系数下降、血液指标异常等,导致25%的小鼠死亡。
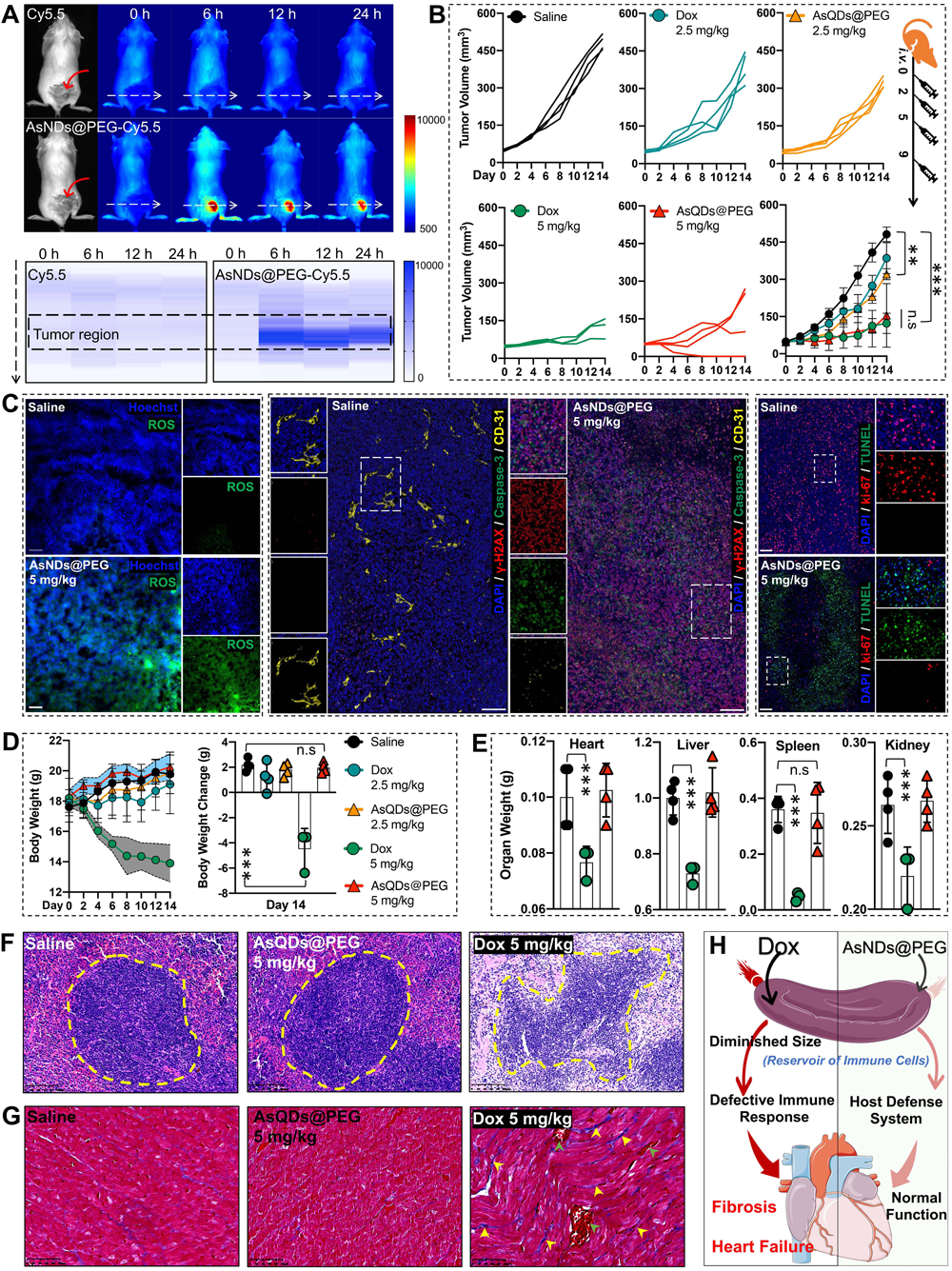
图二 AsNDs@PEG对皮下肿瘤的化疗效果。(A)体内分布;(B)肿瘤曲线;(C)肿瘤免疫荧光切片;(D)小鼠体重;(E)小鼠脏器系数;小鼠(F)脾脏及(G)心脏切片;(H)Dox损伤示意图
随后,作者进一步在小鼠全身性肿瘤转移模型上,验证了AsNDs@PEG对肺转移肿瘤具有一定的化疗效果。临床上通常采用多种化疗药物组合来实现在减少药物剂量的同时,提高治疗效果,减少毒副作用并最大程度降低耐药性。因此,作者进一步探索了AsNDs@PEG联合临床化疗药物的治疗策略。AsNDs@PEG与榄香烯的联合治疗效果协同指数表明,药物联合组在小鼠肿瘤治疗(肿瘤体积及肿瘤质量)取得了显著的协同效应,可实现在荷瘤小鼠层面的低药物剂量的协同高效化疗效果(图三)。

图三 (A-B)AsNDs@PEG对全身性转移模型小鼠的治疗效果;(C)AsNDs@PEG联合榄香烯对荷瘤小鼠的协同杀伤效果;AsNDs@PEG的安全性评价(D)不同给药剂量下小鼠体重及脏器系数的变化,(E)小鼠血液指标,(F)主要脏器H&E病理切片结果
作者将AsNDs@PEG瘤内局部注射后,激光(808 nm, 1.0 W cm-2)照射仅30 s时,肿瘤温度迅速升高至49度,可以在后续的照射时间内达到并维持54-59度;而在注射PBS的小鼠中未观察到明显的温度变化。在接受“AsNDs@PEG + NIR”治疗的小鼠中,成功消融了所有肿瘤,并没有复发迹象。接受仅单次注射AsNDs@PEG的小鼠也显示出有效的治疗效果,肿瘤生长抑制率为77.49%(图四)。
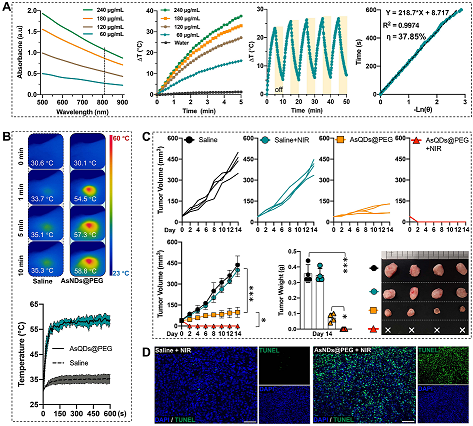
图四 (A)AsNDs@PEG体外光热效果及转换效率;(B)瘤内注射AsNDs@PEG后808 nm激光辐照下升温变化;(C)AsNDs@PEG光热治疗效果;(D)AsNDs@PEG 光热治疗24小时后,肿瘤组织免疫荧光切片
鉴于AsNDs@PEG对实体肿瘤以及转移瘤的治疗效果,以及自身的长期生物安全性,该工作从根本上解决了砷类药物在实体瘤治疗中效果差、毒副作用高等关键瓶颈问题。因此,本研究不仅提供和验证了新型砷药物在实体肿瘤治疗中的可行性,而且阐明了其治疗机制,为以砷烯为代表的新型砷类药物的临床转化提供了基础。
上述论文的第一作者为刘闯博士(现为哈佛大学医学院博士后研究员)、孙山博士(现为江南大学副教授)以及丰强(绍兴文理学院俞樟森博士课题组)。哈佛大学医学院陶伟教授、杭州师范大学药学院谢恬教授与中科院宁波材料所吴爱国教授为该工作的共同通讯作者。
论文信息:Liu C#, Sun S#, Feng Q#, Wu G, Wu Y, Kong N, Yu Z, Yao J, Zhang X, Chen W, Tang Z, Xiao Y, Huang X, Lv A, Yao C, Cheng H, Wu A*, Xie T*, Tao W*. Arsenene Nanodots with Selective Killing Effects and their Low-Dose Combination with ?-Elemene for Cancer Therapy. Advanced Materials 2021, 2102054.
https://doi.org/10.1002/adma.202102054
通讯作者简介:
陶伟,博士毕业于中国清华大学,现任美国哈佛大学医学院助理教授。研究方向主要是围绕药物载体和生物材料的研发及其广泛的生物医学应用(如mRNA/siRNA等核酸递送、肿瘤诊断治疗、心血管疾病、创伤愈合及组织再生、感染或炎症类疾病、糖尿病及其并发症等的治疗等)。陶博士团队研发的多种药物递送核心技术已获系统性的专利、具有良好的产业化背景。近四年以第一作者以及通讯作者身份在Nature Reviews Materials, Nature Reviews Cardiology, Science Translational Medicine, Nature Biomedical Engineering, Matter (Cell Press), PNAS, Nature Communications, Science Advances, Trends in Chemistry (Cell Press), Chemical Society Reviews, Accounts of Chemical Research, Angewandte Chemie, Advanced Materials等期刊上发表论文50余篇,多数论文入选封面论文、Web of Science高被引论文或热点论文。获得美国METAvivor青年研究员奖、美国心脏协会合作科学奖、哈佛大学医学院/布莱根妇女医院纳米医学研究中心基金、系基础科学基金、Khoury Innovation Award、Stepping Strong Breakthrough Innovator Award、哈佛大学医学院助理教授启动基金(Start-up Package)等项目资助。获评《麻省理工科技评论》中国35岁以下科技创新35人(TR35)、微软学术全球Top 5 Trending Authors in Nanotechnology以及Top Authors in Nanomedicine、Elsevier/Mendeley Data全球前2%顶尖科学家榜单(2019年度科学影响力排行榜)、Chemical Society Reviews(IF= 54.564)期刊Emerging Investigator、Materials Horizons(IF= 13.266)期刊Top 10 Outstanding Reviewers等奖项。同时,担任Springer Nature & BMC旗下期刊Journal of Nanobiotechnology(IF= 10.435)副主编,Wiley旗下期刊Exploration副主编,Bioactive Materials(IF= 14.593)、Nano-Micro Letters(IF= 16.419)、Matter(Cell Press, IF= 15.589)等期刊Editorial/Advisory委员会成员,Bioactive Materials (IF= 14.593)、Acta Pharmaceutica Sinica B (IF= 11.413)等期刊客座编辑。
陶伟课题组网页:https://scholar.harvard.edu/wtao/bio
(课题组长期招聘联合培养博士后、博士研究生,欢迎发信联系、期待和大家一起进步!)
谢恬,医学博士,二级教授、研究员,博士生导师,中国农工民主党党员,杭州师范大学医学部药学院院长、整合肿瘤学研究院院长、中西医整合肿瘤防治中心主任、浙江省榄香烯类抗癌药物研究重点实验室主任、浙江省中药资源开发与利用工程技术中心主任、浙八味等浙产中药材综合利用开发浙江省2011协同创新中心主任。谢恬以第一完成人获国家科技进步二等奖2项(2019、2012)、教育部科学技术进步一等奖2项(2018、2008)、中国中西医结合学会科技一等奖(2009)、中国优秀发明专利奖(2013)、吴阶平医药创新奖(2014)、何梁何利科学技术创新奖(2016)、中国发明专利金奖(2019)。谢恬从事中西医结合、现代中药学、脂质体纳米制剂、肿瘤学、绿色化学等科教研与转化近四十年,创新提出中西医结合“分子配伍理论”和“祛邪扶正”治疗癌症及研发抗癌新药。带领团队研发成功我国具有自主知识产权的榄香烯脂质体靶向纳米制剂抗癌新药(榄香烯乳状注射液及榄香烯口服乳),系全球首个上市的脂质体纳米制剂,创建了全球最早的脂质体纳米制剂产业化生产线,开创了倍半萜烯类化合物治疗癌症的先河。已使一百多万癌症患者受益,并帮助2万多户少数民族及山区农民种植温郁金、铁皮石斛、霍山石斛、万寿菊等中药材脱贫致富。发明了降膜式分子蒸馏精制技术及酶法绿色先进技术等用于中药提取活性化合物,解决传统方法生产中药天然药物活性成分高能耗、高污染、品质不佳、纯度不高等难题。创建了濒危珍稀中药铁皮石斛、霍山石斛人工繁育技术及生态栽培体系,为解决濒危珍稀中药资源枯竭,中医临床无药可用的难题创出了一条新路,使中医药及中西医结合可持续发展。
吴爱国,中国科学院宁波材料技术与工程研究所研究员,博士生导师,党委委员,所学术委员会副主任,所属慈溪生物医学工程研究所所长。中共党员,中科院人才,国家JQ。已在Chemical Society Reviews, Advanced Materials, Nano Today,Nano Letters,ACS Nano,Biomaterials等发表论文230余篇,其中封面26篇。申请专利189项(8项PCT),获授权73项(欧美专利各1项)。被引用1.1万余次,H-指数=56。编撰中英文专著4部,受邀撰写专著9章节,是Nanotheranostics,Regenerative Biomaterials等4个学术杂志的编委会成员及Current Medicinal Chemistry的Guest Editor;是全国10个一级学术学会相应15个分会的副主任/(常务)理事,(常务)委员等。牵头制定国家和行业标准各1项。主持科技部重点研发专项课题、NSFC的JQ/联合/面上等项目、中科院先导B专项课题及企业横向委托课题组、医院临床转化中心等30余项。在材料所的研究兴趣集中于:(1)纳米材料的疾病诊疗基础研究与应用;(2)纳米材料在环境科学中的基础研究及应用等。
吴爱国课题组网页:https://wuaiguo.nimte.ac.cn/leader.html
- 杭师大谢恬/浙大孔娜/哈佛医学院陶伟 JACS:榄香烯水凝胶显著抑制癌症术后复发与转移 2024-12-08
- 东华大学史向阳教授团队 Bioact. Mater.:全活性含磷树冠大分子纳米药物通过多靶点免疫调控与神经保护缓解缺血性脑卒中 2026-04-10
- 海南大学吴锡龙教授 AFM:聚焦纳米药物瘤内穿透难题 - 以超声/磁场双引擎驱动实现S型异质结纳米晶的深层肿瘤消融与免疫激活 2026-03-26
- 北京化工大学王兴教授团队《Adv.Healthc.Mater.》:基于双抗生素的pH响应型无载体纳米药物高效治疗混合细菌感染 2025-08-11
- 华南理工大学杜金志教授、都小姣教授 ACS Nano:可注射“特洛伊木马”水凝胶 - 释放可穿透免疫刺激纳米胶束用于胶质母细胞瘤术后治疗 2026-04-20
- 西安交大吴道澄团队 ACS Nano:分子堆砌@无限配位聚合物复合纳米粒实现肿瘤连续高强度光热-热动力交替循环治疗和化疗 2025-08-01
- 巴黎高科化学学院李敏慧教授与合作者 JACS: 创新型“类酶”纳米材料 → 饿死癌细胞 2025-07-20
