缺血性脑卒中(IS)因血管阻塞引发,表现为脑梗死、神经功能缺损与残疾,伴随缺血再灌注损伤,涉及氧化应激、神经炎症、血脑屏障破坏等多重病理机制。缺血区氧化还原失衡促使小胶质细胞向促炎M1表型极化,释放细胞毒性介质,加重神经元与内皮细胞损伤,进一步破坏血脑屏障(BBB)、恶化神经功能。小胶质细胞作为中枢神经系统固有免疫细胞,是应对缺血损伤的关键防线,其表型转化直接影响炎症进程。目前单一靶点药物存在治疗时间窗窄、血脑屏障穿透性差等局限,难以应对复杂病理网络。因此,深入解析IS发病机制,构建安全高效、可同时作用于多靶点的联合治疗策略,对突破现有治疗瓶颈至关重要。
纤连蛋白(FN)是一种重要的细胞外基质糖蛋白,具有调控免疫细胞表型、促进血管生成、减轻炎症反应等多重生物学功能,FN中的精氨酸-甘氨酸-天冬氨酸(RGD)序列可与缺血半暗带内皮细胞上高表达的α5β3整合素选择性结合,从而调控内皮细胞的黏附、迁移和增殖。二十二碳六烯酸(DHA)具备优异的神经保护活性,可通过启动线粒体自噬、调控小胶质细胞极化减轻氧化应激,同时能显著缩小IS中脑梗死范围、改善神经功能。然而,FN存在生物利用度低、易被体内酶降解的问题,DHA则存在水溶性差、半衰期短、细胞膜渗透性不佳,且二者均受BBB高效穿透限制,这些问题严重制约了其临床应用。
纳米平台的开发为解决上述困境提供了新路径。该团队前期研究已证实,羟基端含磷树状大分子不仅拥有良好的生物相容性和结构可设计性,还具备内在抗炎活性,其末端高密度羟基可实现吸附介导的跨细胞转运,助力纳米药物穿透受损的BBB,成功用于阿尔兹海默症、帕金森病的治疗(Nano Today, 2025, 61, 102664;Bioact. Mater.2024, 38, 45-54)。此外,两亲性含磷树冠大分子同时可自组装成稳定的载药纳米胶束,能够延长药物体内循环时间、提高其生物利用度。
基于此,东华大学史向阳教授团队与法国国家科学研究中心Jean-Pierre Majoral院士团队合作构建了羟基端含磷树冠大分子胶束,用于共递送DHA和FN,通过对小胶质细胞、神经元和内皮细胞这三种细胞的三重细胞免疫调节/神经保护/促血管生成作用来缓解IS(图1)。首先,通过发散法合成了带有十个表面羟基和一条疏水性C17H35烷基链的第一代(G1)两亲性含磷树冠大分子,并将其质子化形成阳离子树冠大分子C17G1-OH。该两亲性树冠大分子可自组装形成胶束,有效包裹DHA。随后,FN通过多种物理相互作用与载DHA胶束复合,形成DHA@C17G1-OH/FN胶束。凭借其独特的结构设计与功能优势,可精准作用于小胶质细胞、神经细胞和内皮细胞,通过多重作用机制实现IS的高效治疗。该系统借助羟基端含磷树冠大分子的内在抗炎活性与BBB穿透能力,结合FN介导的靶向递送,可精准将DHA等治疗成分递送至缺血病变部位,不仅有效调控小胶质细胞表型平衡炎症微环境,还可通过激活神经细胞线粒体自噬、减少凋亡,保护神经细胞,促进BBB修复,减少IS大鼠的脑梗死面积、缓解神经损伤。
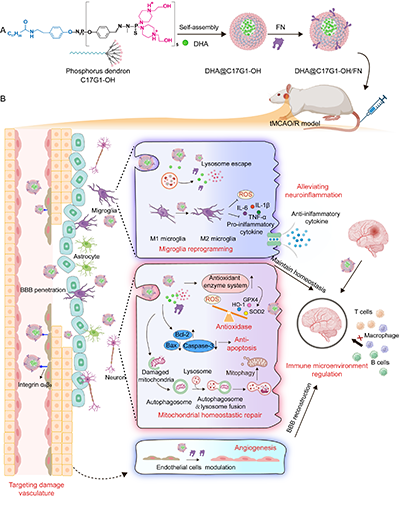
图1. DHA@C17G1-OH/FN 胶束制备及其IS治疗机制示意图。
C17G1-OH含磷树冠大分子胶束装载DHA后呈均一球形形貌(图2A-B),复合FN后胶束形貌保持球形不变(图2C-D),与FN复合前的DHA@C17G1-OH胶束相比,DHA@C17G1-OH/FN胶束的水动力学粒径增至254.5 nm,表面电位从54.98 mV降至11.98 mV(图2E-F),原子力显微镜(AFM)成像检测其高度为54.91 nm(图2G-H)。UV-vis检测进一步证明FN的复合及DHA的装载(图2I)。采用等温滴定量热法(ITC)研究C17G1-OH胶束与FN的相互作用(图2J),结果显示二者结合亲和力强,结合过程主要由疏水相互作用和氢键驱动。同时在模拟体内不同生理环境下,该胶束表现出对低pH及ROS的双重敏感性药物释放行为(图2K)。
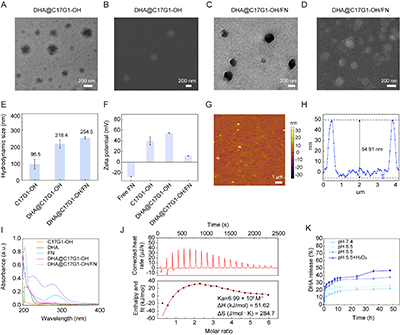
图2. DHA@C17G1-OH/FN胶束的物理化学性能表征。(A)DHA@C17G1-OH胶束的透射电子显微镜(TEM)图像和(B)扫描电子显微镜(SEM)图像。(C)DHA@C17G1-OH/F胶束TEM图像和(D)SEM图像。(E)C17G1-OH、DHA@C17G1-OH和DHA@C17G1-OH/FN胶束的水合粒径及(F)zeta电位。(G)DHA@C17G1-OH/FN 胶束的AFM图像及(H)高度剖面图。(I)C17G1-OH、DHA、DHA@C17G1-OH、FN及DHA@C17G1-OH/FN的UV-vis光谱图。(J)通过ITC分析的C17G1-OH胶束与FN之间的相互作用。(K)不同条件下 DHA的释放情况。
细胞毒性实验表明,DHA@C17G1-OH/FN在DHA浓度达20 μg/mL时,对BV2和SH-SY5Y细胞活力无明显影响,生物安全性良好。体外Transwell BBB模型荧光成像显示,该胶束可有效穿越内皮细胞层递送至下室BV2细胞,FN功能化则显著促进bEnd.3与BV2细胞对胶束的内吞,增强BBB穿透能力(图3A-D)。CLSM成像证实bEnd.3细胞高表达α5β3整合素(图3E),为FN特异性识别提供分子基础,揭示羟基结构与FN整合素识别的双重BBB穿透机制。细胞摄取实验表明,胶束在内皮细胞的摄取依赖巨胞饮及网格蛋白介导途径,受α5β3整合素调控且为能量依赖过程。CLSM与流式细胞分析证实胶束可高效溶酶体逃逸(图3F-H),RGD 肽预处理可使BV2细胞摄取量降低13.0%(图3I)。SH-SY5Y细胞可高效摄取胶束,且胶束经FN靶向识别在细胞质中均匀分布(图3J)。综上,FN功能化通过α5β3 整合素相互作用靶向三大关键细胞,为BBB穿透与IS精准递药提供保障。
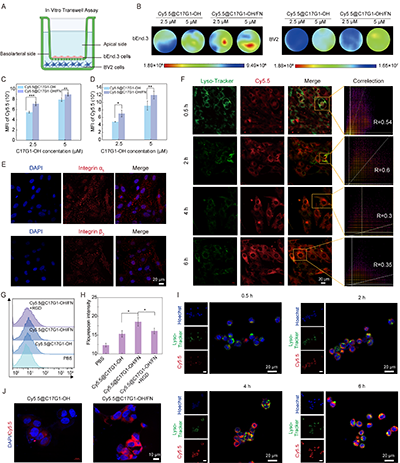
图3. Cy5.5@C17G1-OH/FN胶束的体外BBB穿透及细胞内摄取情况。(A)基于Transwell系统的体外BBB模型示意图。(B)上室(bEnd.3细胞)和下室(BV2细胞)在不同浓度下与Cy5.5@C17G1-OH或Cy5.5@C17G1-OH/FN孵育6小时后的代表性荧光图像。图B中(C)bEnd.3细胞和(D)BV2细胞的定量荧光强度。(E)bEnd.3细胞中整合素α5β3表达的代表性CLSM图像。(F)bEnd.3细胞中Cy5.5@C17G1-OH/FN与溶酶体的共定位及其对应的相关性散点图。(G-H)经不同处理后BV2细胞的材料摄取的代表性流式细胞术图谱及荧光强度。(I)CLSM分析的BV2细胞中Cy5.5@C17G1-OH/FN与溶酶体的共定位情况。(J)SH-SY5Y细胞与Cy5.5@C17G1-OH或Cy5.5@C17G1-OH/FN共孵育4小时后的代表性CLSM图像。
在OGD/R诱导的BV2细胞损伤模型中,研究团队系统验证了DHA@C17G1-OH/FN具有炎症微环境的调控作用。在BV2细胞氧糖剥夺/再灌注(OGD/R)模型中,DHA@C17G1-OH/FN胶束可显著调控小胶质细胞表型,使CD86(M1型)阳性比例降至8.37%,同时大幅提高CD206(M2型)阳性细胞比例,实现强效促M2极化(图4A–B)。ELISA结果显示,该胶束能显著抑制IL-1β、TNF-α、IL-6等促炎因子释放,并促进抗炎因子IL-10生成,抗炎效果显著优于单一组分(图4C–E)。CLSM与流式结果表明,胶束可使BV2细胞内ROS水平降低43.0%,抗氧化能力突出(图4F–G)。
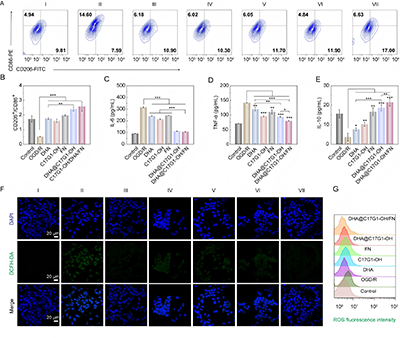
图4. 体外小胶质细胞极化及抗氧化应激作用。(A)不同处理后BV2细胞表型的代表性流式细胞术图。(B)BV2细胞表型CD206/CD86的定量比值。不同处理后BV2细胞上清液中(C)IL-6、(D)TNF-α和(E)IL-10的表达水平。(F)不同处理后BV2细胞内ROS水平的代表性CLSM图像。(G)通过流式细胞术检测的BV2细胞内ROS水平。在图F中,I:对照组;II:OGD/R;III:DHA;IV:C17G1-OH;V:FN;VI:DHA@C17G1-OH;VII:DHA@C17G1-OH/FN。
接下来研究团队进一步评估了DHA@C17G1-OH/FN的神经保护作用。在 SH-SY5Y细胞OGD/R模型中,DHA@C17G1-OH/FN胶束可将细胞凋亡坏死率从52.57%显著降至4.83%,并上调Bcl-2、下调Bax和Caspase-3发挥抗凋亡作用(图5A–C)。同时显著降低细胞内ROS水平,上调GPX4、SOD2、HO-1等抗氧化酶并恢复GSH水平,改善神经元氧化还原稳态(图5D–F)。该胶束可有效激活线粒体保护性自噬,并降低胞内Ca2?浓度,逆转OGD/R导致的钙稳态失衡,最终显著恢复线粒体膜电位,抑制线粒体功能障碍(图5G-K)。整体而言,该体系通过清除活性氧、激活线粒体自噬和维持钙稳态,实现了对缺血损伤神经元的强效保护。
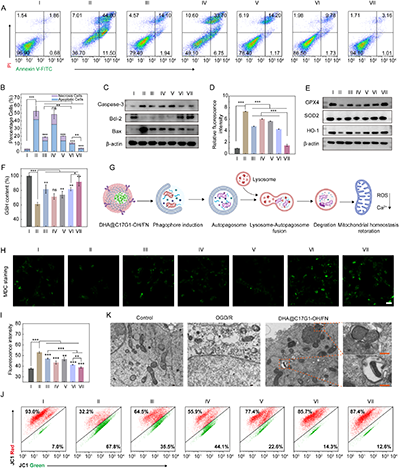
图5. 以OGD/R预处理的SH-SY5Y细胞为模型,研究DHA@C17G1-OH/FN胶束的体外多靶点神经保护作用。(A)细胞与不同药物共培养24 h后凋亡流式细胞术分析图与(B)所得的坏死细胞和凋亡细胞百分比。(C)不同处理后,细胞中Caspase-3、Bcl-2和Bax表达的Western blot分析。(D)不同处理后,细胞ROS的相对荧光强度。(E)经Western blot检测细胞中GPX4、SOD2和HO-1的表达水平。(F)不同处理后细胞中的GSH含量。(G)DHA@C17G1-OH/FN促进线粒体自噬以恢复线粒体稳态的示意图。(H)不同处理后细胞MDC染色CLSM图像(比例尺=20 μm)。(I)不同处理后细胞中Fluo-4 AM的荧光强度。(J)不同处理后,采用JC-1作为探针,对细胞内线粒体膜电位(MMP)进行流式细胞术分析。(K)经DHA@C17G1-OH/FN处理后细胞内线粒体的TEM图像(比例尺 = 200 nm)。
为进一步验证纳米药物的体内BBB穿透和炎症靶向能力,研究团队建立了大鼠大脑中动脉短暂栓塞/再灌注(tMCAO/R)模型。大脑离体荧光成像显示,Cy5.5@C17G1-OH/FN胶束在注射后4、8、24 h均能在缺血侧大脑半球实现显著且持续的荧光富集,效果显著强于Cy5.5@C17G1-OH组(图6A–D),证实FN修饰可显著增强BBB穿透能力并延长在缺血区的滞留时间。组织荧光成像显示,胶束可有效与缺血区血管内皮细胞(CD31)和小胶质细胞(Iba1)共定位,并在缺血敏感的海马区广泛分布(图6E–G),且FN功能化使胶束在细胞内的荧光信号更强、分布更均匀。
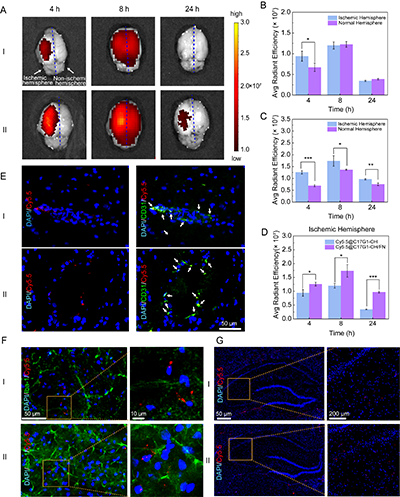
图6. Cy5.5@C17G1-OH/FN在tMCAO/R大鼠体内的脑靶向能力。(A)分别在注射Cy5.5@C17G1?OH和Cy5.5@C17G1?OH/FN后4 h、8 h及 24 h,对tMCAO/R大鼠离体脑组织的荧光成像图。不同时间后,(B)Cy5.5@C17G1-OH和(C)Cy5.5@C17G1-OH/FN组tMCAO/R大鼠缺血半球与正常半球的荧光强度定量分析。(D)两组不同时间点的缺血脑区荧光强度比较。注射后8 h,缺血半球大脑皮层中Cy5.5@C17G1-OH和Cy5.5@C17G1-OH/FN(红色)与(E)内皮细胞,(F)小胶质细胞的共定位以及在(G)海马体中的分布情况。
研究团队进一步按照图7A所示实验方案,对tMCAO/R大鼠模型进行体内给药,并评估不同治疗方式的干预效果。24 h后T2加权磁共振成像和TCC染色结果显示,DHA@C17G1-OH/FN胶束组较其他处理组显著减少脑梗死体积和脑水肿(图7B-D)。伊文思蓝渗漏实验表明,该胶束能最显著抑制BBB渗漏,促进BBB修复并显著改善脑血管密度和结构完整性,重建相互连接的血管网络(图7E–G)。行为学测试中,Zea-Longa神经功能评分显示该胶束组评分多集中在0–1分,疲劳转棒跌落潜伏期较生理盐水组延长50.55s,前肢握力恢复至假手术组的84.25%(图7H–J),可有效恢复大鼠神经和运动功能。综上,DHA@C17G1-OH/FN胶束通过减少脑梗死、修复血脑屏障、重建血管网络及恢复神经功能,展现出优异的IS体内治疗效果。
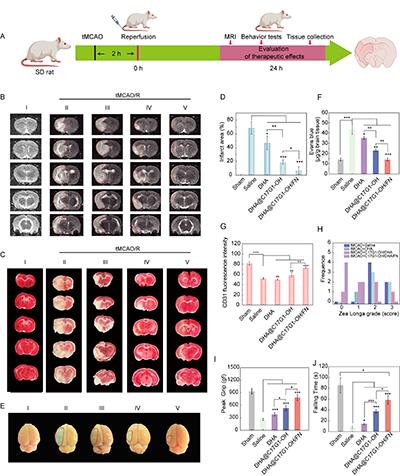
图7. DHA@C17G1-OH/FN在IS大鼠模型中的体内治疗效果。(A)tMCAO/R大鼠的模型建立和给药方案。(B)假手术组大鼠与tMCAO/R大鼠经不同治疗24小时后脑部的代表性T2加权MRI图像,(C)脑切片的代表性TTC染色图像和(D)梗死面积定量。(E)各治疗组在治疗后24小时脑组织中的伊文思蓝渗透图像与(F)伊文思蓝含量的定量分析。(G)经不同处理后受损脑组织中CD31荧光强度的定量结果。(H)经不同处理后tMCAO/R大鼠Zea Longa分级评分(n = 6)。(I)各组在旋转杆测试中的坠落时间。(J)各组前肢抓握张力测试的峰值。在图B、D、E和I中:I:假手术;II:生理盐水;III:DHA;IV:C17G1-OH;V:DHA@C17G1-OH/FN。
H&E染色结果显示,tMCAO/R模型大鼠缺血侧脑组织出现明显核固缩、胞质空泡化与细胞溶解,DHA@C17G1-OH/FN处理后梗死区域显著缩小,核异常与空泡变性基本消失,组织结构接近正常(图8A)。NeuN免疫荧光进一步证实该胶束可有效保护神经元,缺血区神经元荧光分布均匀完整(图8B)。WB分析表明,DHA@C17G1-OH/FN可显著下调促凋亡蛋白Caspase-3、Bax表达,上调抗凋亡蛋白Bcl-2(图8C–D),同时提高SOD2、HO-1、GPX4等抗氧化酶水平(图8E–F)。综上,该胶束通过抑制神经元凋亡、激活内源性抗氧化通路,在体内实现强效神经保护作用。
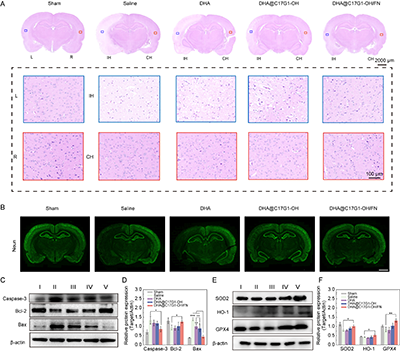
图8. 凋亡抑制与抗氧化防御的分子机制评估。(A)接受不同药物治疗的tMCAO/R大鼠脑组织的H&E染色图。(B)NeuN表达的代表性免疫荧光染色图(比例尺=2000 μm)。(C)不同治疗后缺血脑组织中Caspase-3、Bax和Bcl-2表达的Western blot分析与(D)其定量结果。(E)不同处理后缺血脑组织中SOD-2、GPX-4和HO-1表达的Western blot分析与(F)其定量结果。在图C和E中,Ⅰ:Sharm;Ⅱ:生理盐水;Ⅲ:DHA;Ⅳ:DHA@C17G1-OH;Ⅴ:DHA@C17G1-OH/FN。
免疫荧光结果显示,生理盐水组缺血区Iba1?小胶质细胞呈激活态并与CD68强共定位,而经DHA@C17G1-OH/FN处理后,小胶质细胞向静息态转化,Iba1?/CD68?双阳性比例显著降低(图9A–B)。海马CA1区GFAP染色表明,该胶束可明显抑制星形胶质细胞过度活化(图9C–D);iNOS免疫组化同样显示其能有效降低缺血区炎症活化水平(图9E)。ELISA结果证实,DHA@C17G1-OH/FN可显著下调IL-6、IL-1β、TNF-α等促炎因子,并上调抗炎因子IL-10(图9F–I),通过重编程胶质细胞表型实现神经炎症调控。
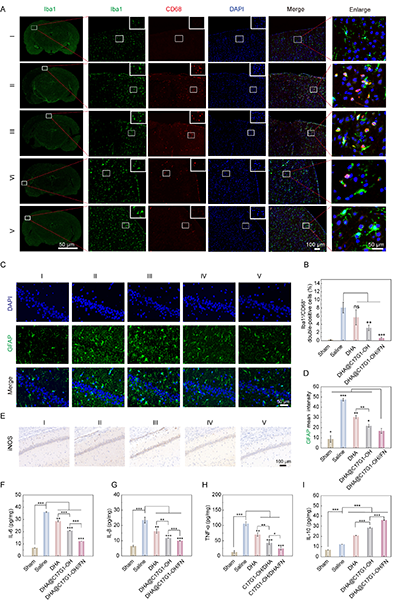
图9. DHA@C17G1-OH/FN胶束的抗神经炎症作用。(A)脑损伤部位Iba1和CD68的代表性免疫荧光图像及(B)及Iba1+/CD68+ 双阳性细胞百分比的定量分析。(C)海马CA1区星形胶质细胞损伤和活化的代表性荧光图像与(D)GFAP表达水平定量分析。(E)海马CA1区iNOS的免疫组化染色。通过ELISA检测缺血脑组织中(F)IL-6、(G)IL-1β、(H)TNF-α和(I)IL-10的细胞因子水平。在图A、C和E中,I:假手术组;II:生理盐水组;III:DHA组;IV:DHA@C17G1-OH组;V:DHA@C17G1-OH/FN组。
IS中发生时,外周免疫细胞大量浸润脑部会加重脑组织损伤。通过流式细胞术分析发现,DHA@C17G1-OH/FN胶束能显著抑制外周单核细胞/巨噬细胞(CD11b?CD45high)、B淋巴细胞(CD19?CD3?)和T淋巴细胞(CD3?CD19?)向缺血脑组织的浸润;同时可有效诱导巨噬细胞表型转换,降低CD11b?CD86?(M1型)细胞比例,提升CD11b?CD206?(M2型)细胞占比,促进巨噬细胞向抗炎修复表型极化(图10A-G);此外,该胶束还能通过修复BBB完整性、减少血管通透性,进一步阻止外周免疫细胞浸润,同时推动巨噬细胞从促炎M1型向抗炎M2型转化,协同减轻神经炎症,为缺血性脑组织修复创造有利条件。
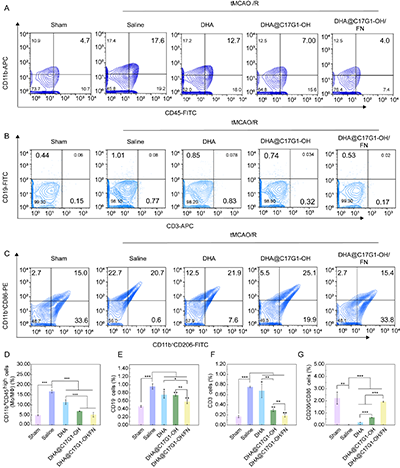
图10. 缺血性脑组织中免疫微环境的调控。(A)不同处理后缺血性脑组织中CD11b+CD45high细胞(巨噬细胞/单核细胞)的代表性流式细胞术图以及(D)其定量分析结果。(B)不同处理后缺血性脑组织中T细胞和B细胞的代表性流式细胞术图以及(E)T细胞和(F)B细胞的相应定量结果。(C)不同处理后缺血性脑组织中巨噬细胞表型的代表性流式细胞术图以及(G)其定量分析。
综上,该研究开发的DHA@C17G1-OH/FN纳米胶束系统具有以下优势:1)通过树冠大分子末端羟基和FN介导的靶向识别实现高效BBB穿透,同时支持FN驱动的内皮细胞调控及后续修复;2)通过含磷树冠大分子、DHA和FN的协同作用促进小胶质细胞M2型极化;3)通过上调抗氧化酶系统和激活保护性线粒体自噬来挽救神经元凋亡;4)通过协同调控IS中上述三种关键细胞类型,实现对IS的多方面干预,包括免疫微环境调控、神经保护、血管生成及BBB重建。所开发的纳米药物结合了生物活性含磷树状大分子载体和多组分药物协同治疗双重优势,为IS的精准、多靶点治疗提供了安全高效的新方案。
以上研究成果以“A full-active phosphorus dendron-based nanomedicine alleviates ischemic stroke through multi-target immunomodulation and neuroprotection.”为题,在线发表于国际著名期刊Bioactive Materials。东华大学生物与医学工程学院史向阳教授为通讯作者,东华大学博士生张彩云第一作者。该工作得到了国家重点研发计划、国家自然科学基金、中国-中东欧国家联合教育项目、上海市科委等项目的资助。
文章链接:https://doi.org/10.1016/j.bioactmat.2026.04.007
- 东华大学史向阳教授团队 AFM:微流控合成无载体全活性的金属酚纳米胶囊用于肿瘤的化疗-化学动力学治疗-免疫治疗 2024-12-02
- 东华大学史向阳教授团队 AM:具有免疫调节功能的含磷树冠大分子载药纳米胶束通过协同调节多种免疫细胞增强肿瘤化学免疫治疗 2022-11-01
- 东华大学史向阳教授课题组 Biomacromolecules:在两亲性含磷树冠大分子纳米胶束用于药物递送上取得新进展 2022-06-15
- 海南大学吴锡龙教授 AFM:聚焦纳米药物瘤内穿透难题 - 以超声/磁场双引擎驱动实现S型异质结纳米晶的深层肿瘤消融与免疫激活 2026-03-26
- 北京化工大学王兴教授团队《Adv.Healthc.Mater.》:基于双抗生素的pH响应型无载体纳米药物高效治疗混合细菌感染 2025-08-11
- 中科大王育才/蒋为团队 Nat. Biomed. Eng.: 利用一氧化氮(NO)突破肿瘤血管基底膜屏障,增强纳米药物瘤内递送 2025-05-03
- 华科大杨光教授团队《Bioact. Mater.》综述:含有生物活性分子和干细胞的载体型水凝胶用于缺血性脑卒中治疗 2025-03-09
