同济大学杜建忠教授提出了高效包载蛋白和核酸的高分子囊泡构建原理:“酸诱导吸附”(Acid-induced adsorption, AIA)和“亲和强化吸引”(Affinity-enhanced attraction, AEA)(图 1、图 2)。
如何利用载体安全有效地递送生物大分子,是蛋白疗法、组织修复、基因编辑等生物医用领域的一个核心问题。然而传统载体往往带正电荷,体循环时间较短且存在安全问题。虽然非阳离子载体可以避免这个问题,但是包载效率较低。高分子囊泡可将大分子包载在空腔中,安全性好,但长期以来同样面临包载效率较低的难题。因此,如何构建高效包载生物大分子的非阳离子型高分子囊泡是一个重要的挑战,需要从理论创新方面来解决问题。
杜建忠教授团队长期以来一直从事高分子囊泡包载生物大分子的研究【“人工核膜”囊泡(ACS Nano 2014, 8, 5022);“以糖控糖”囊泡(JACS 2017, 139, 7640);“双门控”囊泡(Nano Lett. 2018, 18, 5562)】。他们猜想,要实现生物大分子的高效包载,核心在于调控囊泡与生物大分子之间的相互作用。在溶液中,生物大分子通过被动扩散靠近囊泡。通常情况下,由于二者之间的相互作用较弱,大多数大分子会离开囊泡。而当二者之间的吸引作用较强时,就可以将大多数大分子吸附在囊泡膜上,实现大分子捕获,即“稳定包载”。根据该猜想,他们提出了AIA和AEA原理以高效包载蛋白和核酸。
他们设计了一种新的高分子囊泡以验证上述原理。实验表明,通过AIA使血红蛋白包载率达到了79%,通过AEA使RNA和质粒DNA包载率分别达到了85%和75%。这些结果均大大高于普通的高分子囊泡的包载效率(一般小于20%),主要是因为AIA和AEA的 “主动包载”作用(图 1)。
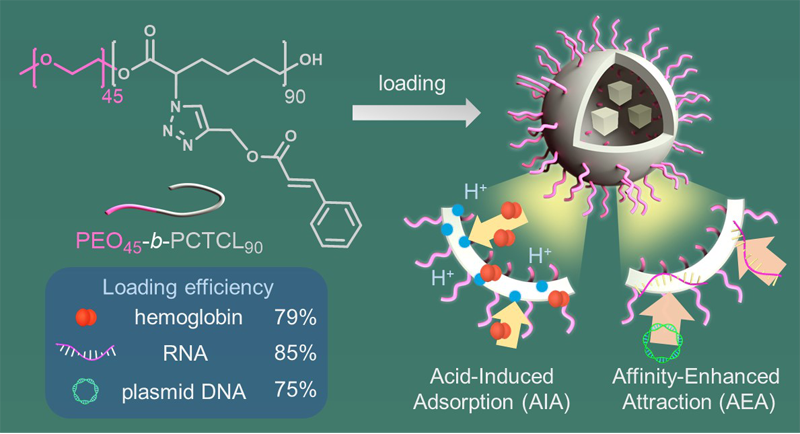
图 1. 高效包载蛋白和核酸的原理:酸诱导吸附(AIA)和亲和强化吸引(AEA)
AIA:蛋白溶于水产生的质子可以被三唑基团中氮原子的孤对电子吸引,进而催化囊泡膜层的酯键断裂,所形成的羧基和羟基可以通过静电作用或氢键作用吸附蛋白分子,进而实现蛋白的高效包载(图 2)。
AEA:高分子侧链上的三唑基团和肉桂酸酯基团可以通过“π–阴离子作用”和“π–π堆叠”吸引带负电且富含π电子的核酸分子。另外,高分子侧链与核酸的重复单元有一定的结构相似性,进一步加强了二者之间的吸引作用。这些因素都有利于核酸的高效包载。

图 2. 囊泡通过(I)AIA和(II)AEA分别包载蛋白和核酸的示意图
在包载编码有绿色荧光蛋白基因的质粒后,囊泡可以将质粒高效递送至细胞内进行表达。激光共聚焦测试表明,AEA不影响大分子的胞内释放与表达,与对照组(纯质粒组)相比,荧光强度提高两倍以上(图 3)。进一步实验证实,包载质粒的囊泡对于人肝癌细胞(HepG2)的转染效率在95%以上(72小时)。由此可知,AEA在基因递送领域具有应用前景。
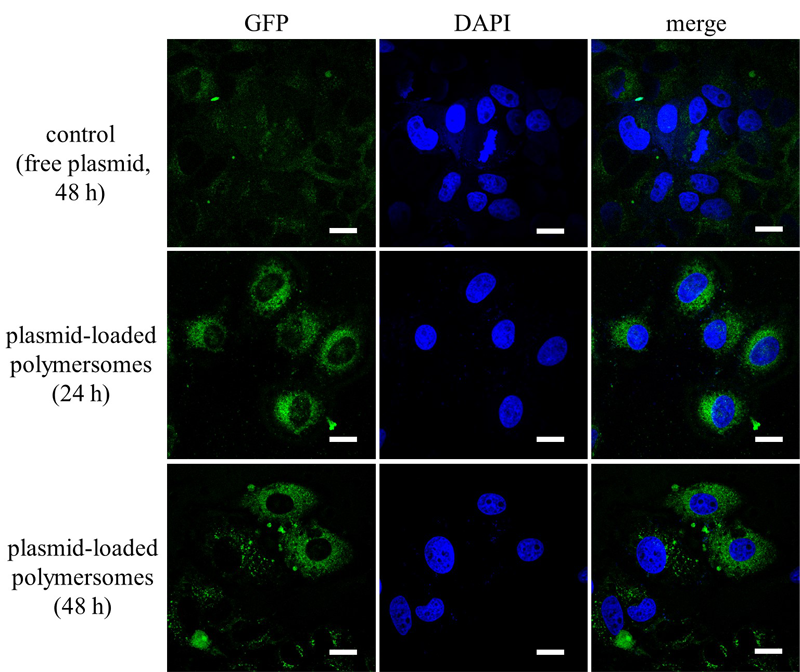
图 3. 包载pEGFP-N1质粒的囊泡有效实现了基因递送和表达(绿色:荧光蛋白;蓝色:细胞核;比例尺:20微米)
AIA原理可以扩展到具备如下几个特点的载体体系:1)体系中有质子源以催化高分子链中酸敏感键的降解;2)载体中包含具有孤对电子且均匀分布的助催化剂,用于质子的传递和分散;3)载体膜中具有酸敏感的化学键,在断裂后暴露出的基团,能够与“货物”分子产生氢键或静电作用。
AEA原理适用于具备以下任一特点的载体体系:1)载体的膜结构包含对“货物”分子中的富电子基团或带负电荷基团具有亲和作用的基团;2)载体的膜结构中有富含π电子的基团,可以促进载体膜与“货物”分子之间产生“π–π堆叠”作用。另外,当聚合物中含有与大分子“货物”重复单元相似的化学结构时,AEA效应可以进一步增强。因此,可将AIA、AEA推广到其他领域。
该成果以“Two Principles for Polymersomes with Ultrahigh Biomacromolecular Loading Efficiencies: Acid-Induced Adsorption and Affinity-Enhanced Attraction”为题发表(Macromolecules 2020, DOI: 10.1021/acs.macromol.0c00252)。同济大学博士生陈帅为论文的第一作者,河北大学秦江雷副教授为第二作者,同济大学杜建忠教授为通讯作者。该研究得到国家杰出青年科学基金(21925505)资助。
论文原文:
Chen, S.; Qin, J. L.; Du, J. Z.* Two Principles for Polymersomes with Ultrahigh Biomacromolecular Loading Efficiencies: Acid-Induced Adsorption and Affinity-Enhanced Attraction. Macromolecules 2020, DOI: 10.1021/acs.macromol.0c00252.
https://pubs.acs.org/doi/abs/10.1021/acs.macromol.0c00252
杜建忠教授课题组主页:https://jzdu.tongji.edu.cn/
- 河南大学《Adv. Sci.》:高分子囊泡弹性对脑肿瘤靶向影响研究新进展 2021-09-02
- 同济大学杜建忠教授课题组提出氨基酸环内酸酐开环聚合诱导自组装(NCA-PISA)新方法 2019-09-17
- 同济大学杜建忠教授课题组“以糖控糖”高分子囊泡新进展 2019-07-11
- 武汉大学陈朝吉/余乐 Natl. Sci. Rev.:可回收电凝胶化生物大分子水凝胶电解质助力可持续宽温域锌金属电池 2025-08-11
- 苏州大学李刚教授、美国国家标准与技术研究院Wai Cheong Tam博士 IJBM:牙周组织生物大分子研究进展 2025-05-22
- 苏大李刚、余嘉/港理大赵泽宇 Int. J. Biol. Macromol.:伤口修复生物大分子材料的研究进展 2024-04-03
