类风湿关节炎(RA)是一种慢性自身免疫性疾病,以关节滑膜炎症、软骨磨损和润滑功能丧失为特征。现有治疗方法(如抗炎药物注射和关节润滑剂补充)存在药物滞留时间短、重复注射风险高、无法同时解决炎症和软骨损伤等问题。传统水凝胶或侧重抗炎,或侧重润滑,难以实现长效关节保护和组织修复。因此,开发一种兼具抗炎、润滑、粘附和软骨修复功能的创新疗法迫在眉睫。
针对以上难题,西南交通大学鲁雄/谢超鸣团队和苏州大学李斌/林俊团队联合报道了一种可注射的生物粘合-润滑水凝胶。该水凝胶主体是由负载KGN的多巴胺(DA)衍生碳量子点支撑的铜单原子纳米酶(DAGQD@Cu@KGN SAN)以及多巴胺修饰的透明质酸(DA-HA)和磺酸根修饰的透明质酸(SO3--HA)构成。该研究创新性地将仿生高分子网络与单原子催化技术深度融合,开发出兼具粘附-润滑-再生三重功能的可注射水凝胶。其创新点在于:① 多酚介导的单原子铜纳米酶,通过原子级分散的Cu活性中心与儿茶酚-醌氧化还原循环,实现超氧化物歧化酶、过氧化氢酶和羟基自由基清除的三重催化活性;② DA-HA/SO3--HA双网络动态交联设计,结合贻贝仿生粘附与滑液仿生润滑,解决传统材料粘附弱、易流失的难题;③ KGN功能化缓释系统,通过酰胺键精准负载软骨诱导因子,实现长效释放,同步招募干细胞并促其分化为软骨细胞。

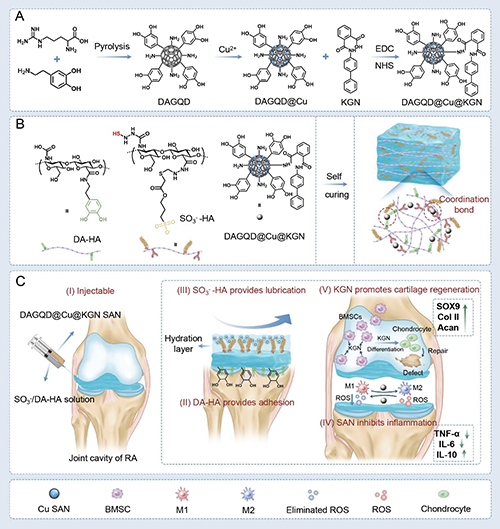
图1. 水凝胶合成与RA治疗机制示意图。(A)DAGQD@Cu SAN与DAGQD@Cu@KGN SAN的合成路径;(B) DAGQD@Cu@KGN-SO3-/DA-HA水凝胶的构建过程;(C)水凝胶在RA治疗中的多功能作用:I 关节腔内原位自固化;II-III 润滑与粘附性能;IV SAN介导的ROS清除与抗炎;V KGN释放促进BMSCs分化为软骨细胞
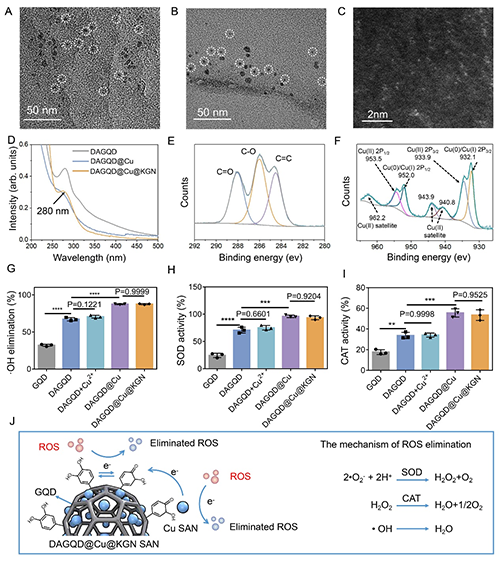
图2. 单原子纳米酶(SAN)表征。(A)DAGQD@Cu SAN与(B)DAGQD@Cu@KGN SAN的透射电镜(TEM)图像;(C)高角度环形暗场扫描透射电镜(HAADF-STEM)图像显示铜单原子分散;(D)UV-Vis光谱对比:DAGQD、DAGQD@Cu SAN与DAGQD@Cu@KGN SAN;(E-F)XPS分析:C1s(E)与Cu2p(F)谱图;(G-I)纳米酶的羟基自由基清除能力(G)、SOD活性(H)与CAT活性(I)
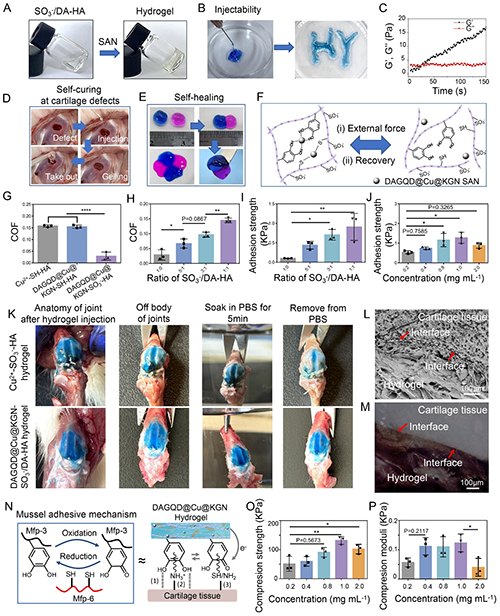
图4利用水凝胶与LPS、 H2O2分别与巨噬细胞共孵育进一步证明了水凝胶具有良好的ROS清除能力,这不仅是因为DAGQD@Cu@KGN-SO3-/DA-HA水凝胶上有丰富的邻苯二酚基团,而且还因为Cu单原子纳米酶具有多种ROS清除和酶催化活性。同时水凝胶还具有良好的抗炎能力,可下调促炎因子TNF-α、IL-6的表达,对抑炎因子 IL-10 的表达有促进作用。DAGQD@Cu@KGN-SO3-/DA-HA水凝胶还可促进骨髓间充质干细胞(BMSCs)的增殖、粘附和分化,促进软骨相关标记物Sox9、Acan和 Col II的基因表达水平,证明其具有促软骨生成能力。

图4. 体外生物学性能.(A-B) 细胞内氧水平(RDPP荧光成像与流式分析);(C-D )巨噬细胞ROS清除效果(DCFH-DA染色与流式定量);(E-G) ELISA检测炎性因子TNF-α(E)、IL-6(F)与抗炎因子IL-10(G);(H) BMSCs在不同水凝胶上的增殖(CCK-8测试);(I) BMSCs粘附形态(荧光染色);(J-M) 软骨分化标志物(Sox9、Acan、Col II、Col X)的基因表达

图5 RNA测序分析。(A-B)差异基因火山图(Group 2 vs. Group 1与Group 3 vs. Group 1);(C)差异基因韦恩图;(D)GO功能富集分析(抗氧化、自噬、修复相关通路);(E)GSEA通路分析:FoxO信号、溶酶体、破骨细胞分化与TNF通路;(F)热图展示抗氧化、自噬、修复与炎症相关基因表达;(G)水凝胶作用机制整合示意图
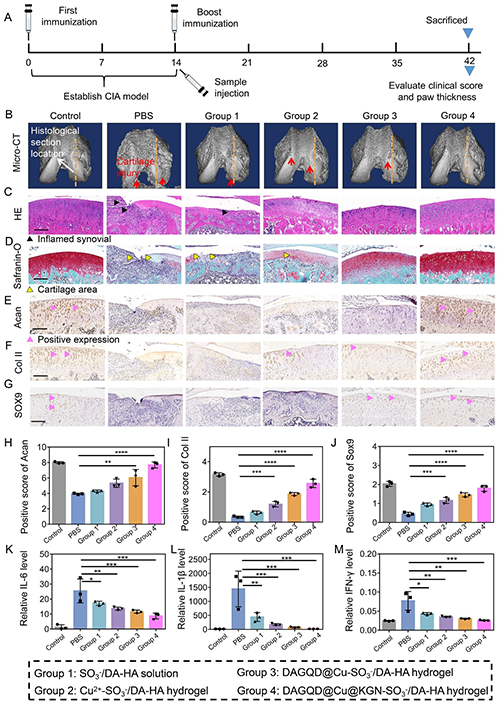
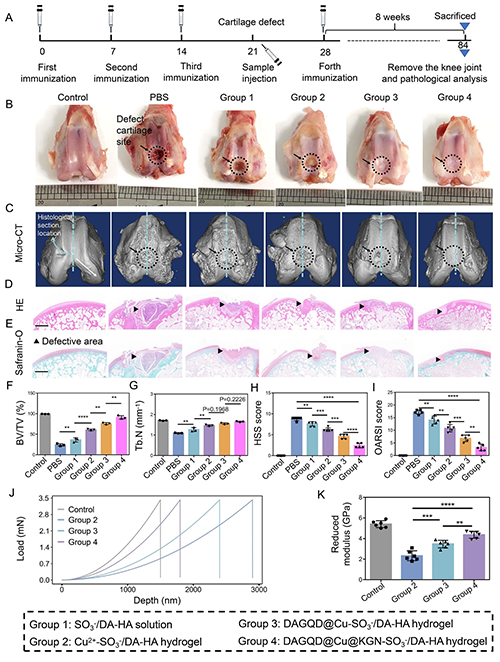
图6. 早期RA大鼠治疗效果。(A)实验流程示意图;(B)Micro-CT三维重建显示关节骨破坏程度;(C-D)组织学染色(H&E与Safranin-O)评估软骨完整性;(E-J)免疫组化与定量分析:Sox9、Col II、Acan表达水平;(K-M)血清炎性因子(IL-6、IL-1β、IFN-γ)浓度检测
原文链接:https://www.nature.com/articles/s41467-025-58059-z
- 浙大王征科课题组《Macromol. Rapid Commun.》: 泥鳅粘液-甲基丙烯酰化明胶超润滑水凝胶 2025-06-30
- 兰州化物所王晓龙研究员团队 AFM:利用低熵纳米晶域网络构建的机械鲁棒性润滑水凝胶 2025-05-14
- 中南林科大吴献章团队 AFM:溶剂诱导的动态键调控策略制备生物质自适应润滑水凝胶 - 用于智能调速 2024-10-19
- 中国海大孔明、烟大陈大全《Int. Biol. Macromol.》:牛膝多糖“引药下行”双重响应纳米药物递送治疗类风湿关节炎 2023-02-25
- 湖南工业大学汤建新和厦门大学聂立铭团队:纳米药物治疗类风湿关节炎的最新进展 2020-06-01
- 中山大学陈永明教授和刘利新副教授团队在聚合物材料抑制类风湿性关节炎的研究中取得重要进展 2018-10-26
