浙江大学计剑、张鹏团队 JACS:选择性细胞阻抗调控细胞-材料界面相互作用
2025-03-07 来源:高分子科技
调节不同类型细胞在材料-组织界面的行为是诱导组织再生的关键。传统的方法是利用特定的配体(如多肽和抗体)来增强靶细胞的结合性,但这些配体在生物环境中存在稳定性问题,限制了其临床应用。

该成果于2025年3月4日以“Regulating Cell–Material Interfacial Interactions through Selective Cellular Resistance”为题发表于《Journal of the American Chemical Society》,浙江大学博士后郝鸿业和博士生陈怡峰为论文共同第一作者。
调节不同类型细胞在植入物表面的行为,在组织再生和过度增生之间取得平衡是改善植介入手术预后的关键。传统策略往往利用特定配体,如多肽和抗体,来选择性地与细胞膜上的相应受体作用,从而提升靶细胞的结合性。但该策略受限于配体分子在生理环境中的不稳定性,难以实际应用。因此,作者提出猜想:是否能够反其道而行,通过选择性细胞阻抗来实现靶细胞的选择性粘附?
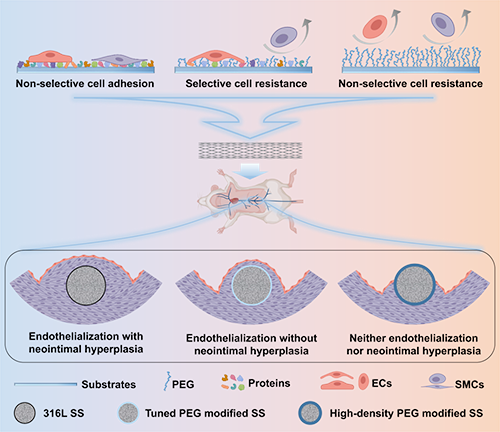
图1 选择性细胞阻抗调控细胞-界面相互作用示意图。
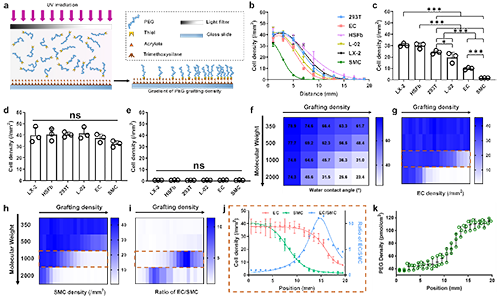
图2 选择性细胞阻抗表面的制备与筛选。
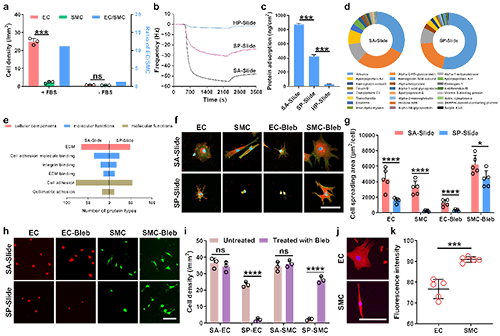
图3 SMC选择性阻抗机理探究。
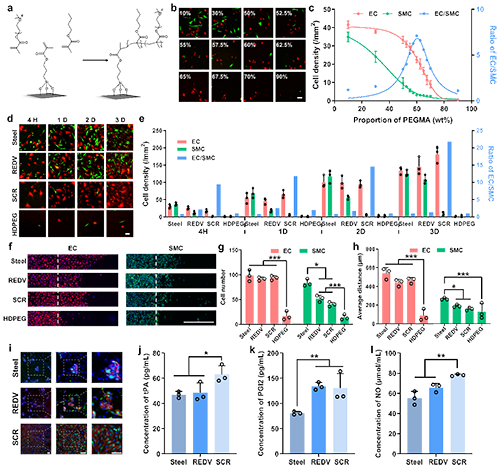
图4 SMC选择性阻抗聚合物涂层对细胞粘附、增殖、迁移、内皮化的影响。
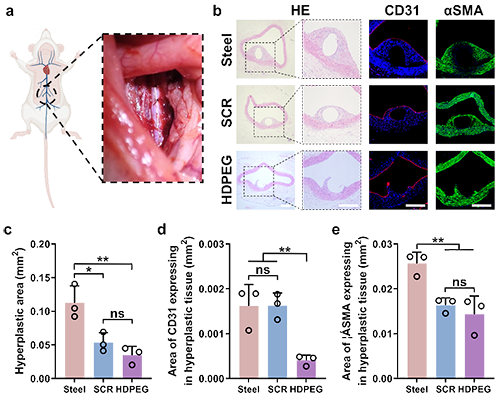
图5 SMC选择性阻抗聚合物涂层的体内促内皮化与抑制内膜增生效果。
原文链接:https://pubs.acs.org/doi/10.1021/jacs.5c01433
版权与免责声明:本网页的内容由中国聚合物网收集互联网上发布的信息整理获得。目的在于传递信息及分享,并不意味着赞同其观点或证实其真实性,也不构成其他建议。仅提供交流平台,不为其版权负责。如涉及侵权,请联系我们及时修改或删除。邮箱:info@polymer.cn。未经本网同意不得全文转载、摘编或利用其它方式使用上述作品。
(责任编辑:xu)
相关新闻
- 中山大学元辛、顾林团队 PMS 综述:界面相约束效应 - 二维材料增强聚合物涂层的多尺度机制和工程突破 2026-05-08
- 川大姜猛进/喻媛媛 Small:海绵状多孔离子/电子双导体聚合物涂层制备超稳定的硅负极用于锂离子电池 2023-07-27
- 上海电力大学曹怀杰《Prog. Org. Coat.》:二维材料复合防腐涂层取向调控与表征策略综述 2023-06-05
- 哈工大冷劲松/哈医大郭媛媛 AFM:抗凝促内皮化4D打印心脏封堵器 2026-04-01
- 苏大李刚、附四院张喜成团队 Biomacromolecules: 抗凝血和促内皮化功能的血管覆膜支架 2025-09-25
- 四川大学王云兵教授/罗日方副研究员Biomaterials:微创介入式生物瓣膜材料改性实现长效抗凝及内皮化增强的新策略 2021-06-29
