具有可控降解性能的聚合物是高分子科学的一个重要研究领域,近年来受到广泛关注。在一些医学应用场合,需要可控降解的聚合物,但存在的主要挑战是聚合物降解速率的可控性,降解产物的生物安全性等。尽管在生物医学领域,可降解高分子材料的研究取得了一些重要的进展,但仍需开发更优的可控降解的聚合物,来满足应用需求。
近日,浙江大学张兴宏教授/张成建研究员团队,以希夫碱和环酸酐为单体,在无催化剂的温和条件下,合成得到了多种不同结构的自动降解的共聚物。其中,希夫碱单体由芳香醛和伯胺一步缩合得到,环酸酐则是由二元酸脱水得到,大部分可直接购买。希夫碱和环酸酐按照1:1.1投料比在二氯甲烷中溶解,在20-50℃发生共聚反应,得到了大环结构、完全交替序列的共聚物。作者推测两单体反应生成两性离子,以两性离子机制共聚,。这一策略成功拓展到10种希夫碱和6种环酸酐的共聚合,共计合成得到了15种共聚物。所得共聚物的重复单元含酯基和类肽(N-取代酰胺)结构,数均分子量(Mn)为1.8-16.8 KDa,分子量分布(?)为1.2-1.8,玻璃化转变温度(Tg)为27-77 ℃,初始热分解温度介于120℃至175℃之间,依据共聚物结构不同而不同。
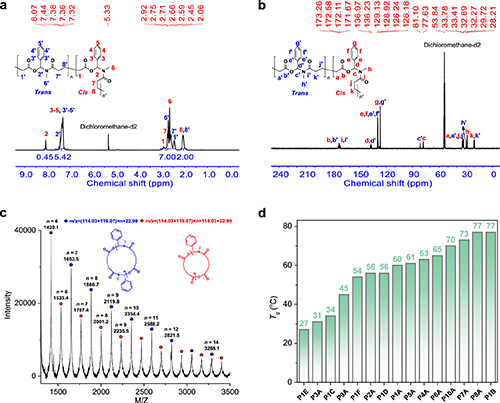
图1.所得共聚物的结构分析和热性能
有趣的是,这些聚合物在无外界触发条件下,完全降解成内酰胺小分子。从最终产物来看,这正是环酸酐与亚胺环加成反应(即Castagnoli-Cushman反应)的产物。重要的是,这些共聚物的降解速度可以通过分子结构、储存条件来调控,完全降解为小分子的时间为几小时到几个月不等。例如图1中的共聚物(起始原料为乙胺、苯甲醛得到的席夫碱、戊二酸酐)在0℃下储存30天,其分子量几乎没有变化,表明其在低温条件下具有较好的稳定性,为其储存和应用提供了便利。
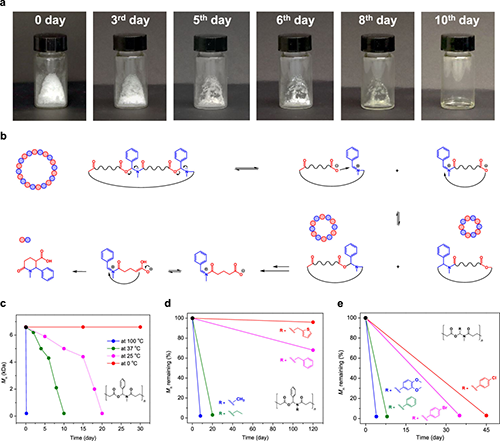
图2.所得共聚物的降解研究
作者采用上述共聚物为缓释药物载体,展示了其可控降解性质的潜在应用。研究团队通过水/油/水溶剂蒸发的方法,制备了负载了雷帕霉素(雷帕霉素是一种免疫抑制剂,难溶于水、在水中不稳定,应用时常需要大量给药和频繁注射)的共聚物纳米颗粒,纳米粒子载药量为16%,包封率为94%。体外释放实验结果表明,在25℃时,雷帕霉素可从纳米颗粒中缓慢释放出来,15天内释放了约90%的药物;当温度升高至37℃时,药物释放速度显著加快,3天内释放了90%的药物。这一结果与共聚物降解的规律一致,即温度越高,共聚物降解越快,相应的,药物释放的速度也越快。进一步的药代动力学研究表明,单次尾静脉注射雷帕霉素或负载雷帕霉素的共聚物纳米颗粒后,负载药物的纳米颗粒在小鼠血清中的药物浓度较单独使用雷帕霉素的浓度更高,表明该策略能够有效延长药物在体内的循环时间,实现缓释效果。同时,共聚物及其降解产物对NIH3T3细胞无毒性。
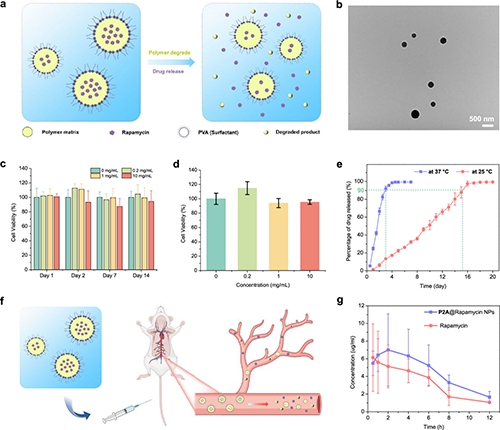
图3.可自降解聚合物作为载体材料以实现药物持续释放
综上,作者展示了一类新的可控降解聚合物,具有希夫碱和环酸酐交替的重复单元和环状拓扑结构,初步展示了这些共聚物组装物在体内外的降解性和作为药物载体的潜力。本文结果为设计可控降解的聚合物提供了新的思路。
这一研究结果以“Autodegradable Polymers: Complete Degradation without Any Trigger, Tunable Performance, and Biomedical Applications”为题发表在《Journal of the American Chemical Society》上,浙江大学高分子系博士生陈铄泓为本文第一作者,张成建研究员和张兴宏教授为本文通讯作者。该工作得到了国家自然科学基金项目的资助。
原文链接:https://doi.org/10.1021/jacs.4c14077



