
随着人口老龄化的加剧,心脑血管疾病,糖尿病,肥胖等疾病的发病率越来越高,进而导致的压疮、褥疮,甚至其他慢性溃疡创面越来越多。传统的伤口敷料,如纱布,已经不能满足慢性伤口的愈合需求。水凝胶敷料在医学领域虽已被广泛研究,但其强力低不适用于需要强力支撑的活动部位,此外还具有透气性差等缺点。静电纺丝膜的无序排列也不具备靶向给药的问题,这些都限制了材料的实际应用。因此,开发一种具有定向给药并且具有一定强度的伤口敷料具有重要意义。基于此,天津工业大学李婷婷副教授与台湾逢甲大学林佳弘特聘教授和台湾亚洲大学楼静文特聘教授合作,在前期对微流控纺丝制备定向纤维膜的研究基础上(Colloid Surface B 2023,229,113442),利用同轴微流控法构建皮芯结构载药有序定向纤维膜,研究成果以“Coaxial Microfluidic Spinning Design Produced High Strength Alginate Membranes for Antibacterial Activity and Drug Release”为题发表在期刊《International Journal of Biological Macromolecules》。

Figure 1. Scheme illustration of (a) the preparation of ZIF-8/AA and (b) the core-shell alginate functional membrane using coaxial microfluidic spinning.

Figure 2. (a) coaxial microfluidic spinning (a’) SA/ZIF-8/AA microfluidic membrane (a’’) SA/ZIF-8/AA microscopic view (′ 60 times); (a’’’) lightweight of the modified membrane; (b)~(g) the influence of microfluidic wet spinning parameters on mechanical properties; (h) the cross section of SA/ZIF-8/AA membrane; (i) FTIR spectrum of SA/ZIF-8/AA with different content of ZIF-8/AA; (j) EDS of SA/ZIF-8/AA membrane.

Figure 3. The qualitative and quantitative assessments of the SA/ZIF-8/AA oriented membrane (A) the photos of bacteria colonies antimicrobial performance of the membranes; (B), (C) the quantitative analysis of the bactericidal performance of the membrane against two bacteria; (D) mechanism of the antibacterial properties of ZIF-8 nanomaterials; (E), (F) the release of reactive oxygen species from the membrane

Figure 4. The drug release of synthesized ZIF-8/AA at different pH values (a) the standard curves of AA concentration and corresponding absorbance; (b) the drug release efficiency within 8 hrs.; (c) the first order fitting curve; (d) the second order fitting curve model at different pH values; (e) Higuchi models at different pH values; (f) Korsmeyer-Peppas models at different pH values
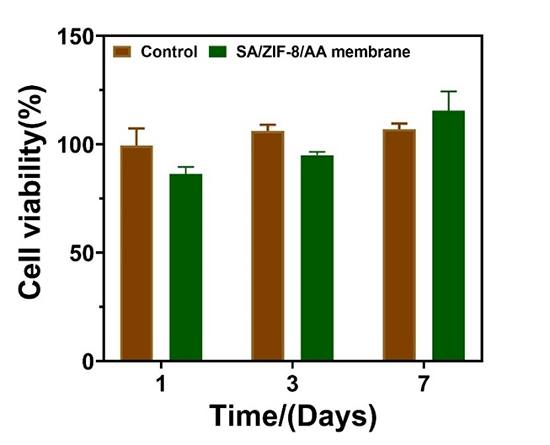
Figure 5. In vitro cytotoxicity of the SA membrane loaded ZIF-8/AA co-cultured with L929 cells
本研究通过同轴微流控纺丝法构建载药抗菌有序微结构纤维膜,为多功能创面敷料的制备提供了一种思路。论文的第一作者为天津工业大学纺织科学与工程学院张莹博士,天津工业大学李婷婷副教授和台湾亚洲大学楼静文特聘教授为论文的通讯作者。该研究得到国家自然科学基金、中国纺织工业联合会研究基金和福建省自然科学基金的支持。
原文链接:https://doi.org/10.1016/j.ijbiomac.2023.124956
- 青岛大学牛海涛、周华教授团队 IJBM:天然植物基、无氟多功能涂层织物的构建与性能研究 - 集高牢度超疏水、抗菌与抗氧化于一体 2026-03-13
- 四川大学孙静/范红松团队 ACS Nano:兼顾抗菌活性与细胞保护功能的类酶水凝胶用于细菌性角膜炎中的角膜再生 2026-03-05
- 东华大学朱美芳教授、贾超副研究员等 AFM:抗菌、制冷多功能聚乙烯纤维防护材料 2026-01-06
- 王晓强/孙燕/孙耀/Peter J. Stang院士 PNAS:基于金属-有机环/笼的细菌响应多层创面敷料促进伤口愈合 2024-04-02
- 郑州大学关方霞教授、姚明浩副教授团队 ACS AMI:可注射、自愈合、组织粘附性多功能水凝胶用于快速止血和伤口愈合 2022-07-23
- 苏大李刚、郑兆柱和苏大附一院李峰合作 ACS BSE: 丝素蛋白基药物缓释功能输尿管支架 2023-12-27
- 复旦大学舒易来/王武庆/商珞然团队合作 ACS AMI:开发耳聋治疗新型药物缓释载体 2022-10-17
