东华大学史向阳教授课题组 Biomacromolecules:在两亲性含磷树冠大分子纳米胶束用于药物递送上取得新进展
2022-06-15 来源:高分子科技
优良的药物传递系统可以有效地克服抗癌药物与正常细胞的非特异性结合和水溶性差等问题。在众多的纳米药物递送系统中,脂质体、纳米凝胶、聚合物-药物缀合物、树状大分子、树冠大分子、胶束和无机纳米颗粒在纳米医学的发展中获得了广泛关注。其中,胶束因其独特的优势而备受青睐:1)药物负载能力强,可通过改善药物的药代动力学/药效学特征来提升治疗效果;2)体积小(< 30 nm),可有效穿透至肿瘤深部组织;3)可与特定配体(如适配体)结合实现主动性肿瘤靶向。胶束一般是由两亲性的小分子或聚合物组成。然而,基于两亲性小分子构建的胶束稳定性有限,而基于两亲性聚合物构建的胶束则存在分子量分布不均一的问题。因此,如何构建一类药物包封率高、结构稳定、生物相容性佳的给药系统对于肿瘤治疗具有特殊意义。
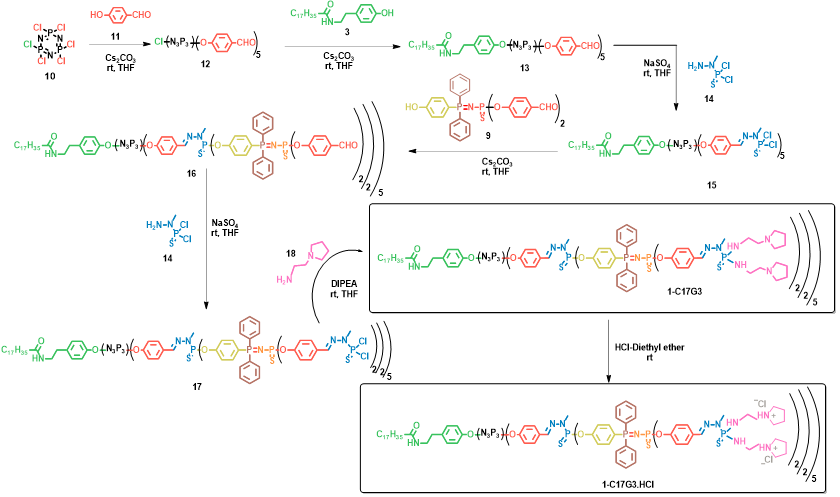
图 1. 两亲性含磷树冠大分子的合成示意图
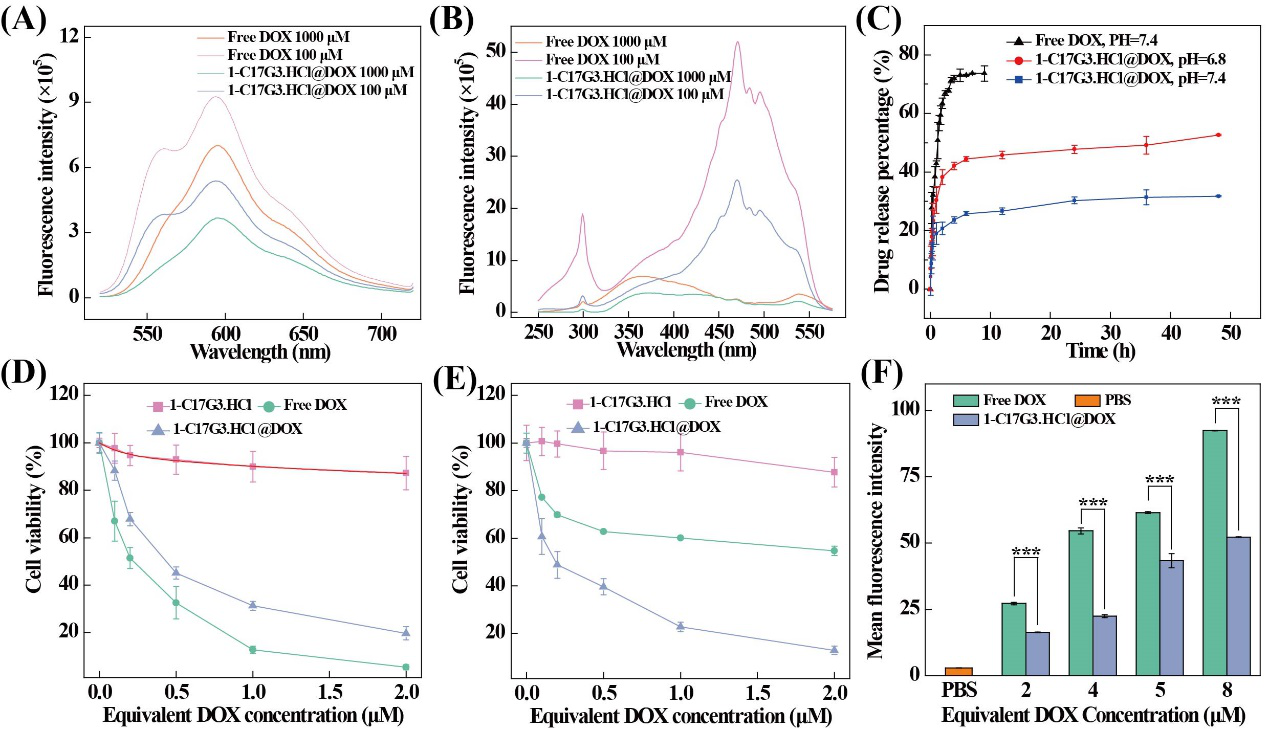
图 2. 1-C17G3.HCl@DOX和free DOX的稳态荧光发射(A)和激发(B)光谱(DOX浓度为100 μM和1000 μM,激发波长=365 nm,发射波长=595 nm);(C)负载DOX的纳米胶束1-C17G3.HCl@DOX 在不同pH条件下的药物释放动力学曲线。自由的DOX在pH = 7.4条件下的释放作为对照。NIH-3T3 (D)和MCF-7(E)细胞毒性测试结果;(F)流式细胞术检测不同相对DOX浓度条件下细胞对纳米胶束的吞噬量。
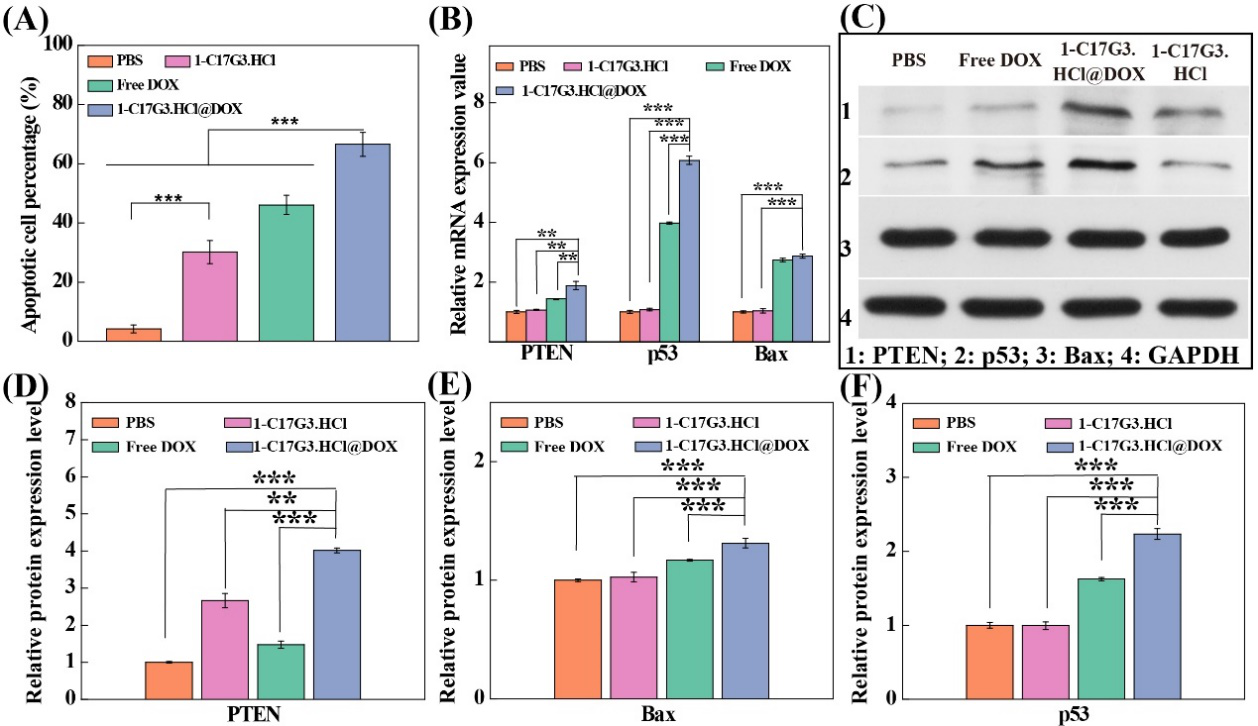
图 3. (A)细胞凋亡百分比的直方图;(B)PTEN、p53和Bax基因的相对表达量;(C)PTEN、p53和Bax的蛋白质印迹分析结果;(D-F)蛋白质印迹的定量分析直方图。
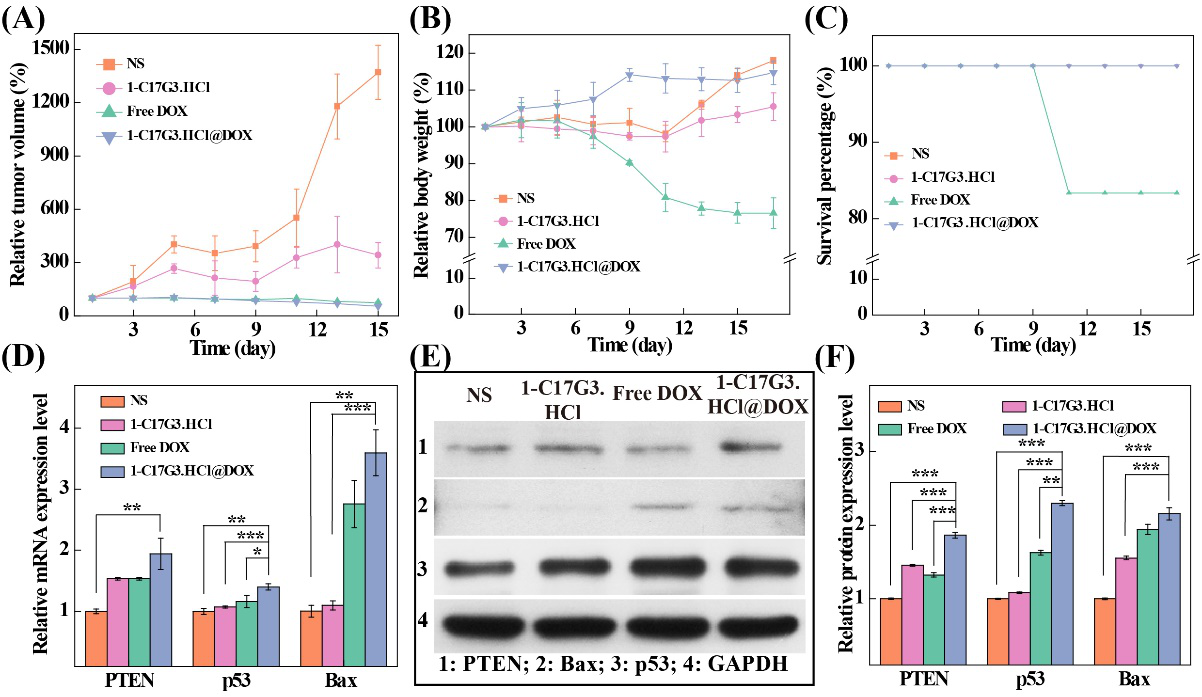
图 4. (A)肿瘤相对体积变化;(B)裸鼠相对体重变化;(C)裸鼠存活率变化;(D)肿瘤组织中PTEN、p53和Bax基因的相对表达量;(E)PTEN、p53和Bax的蛋白质印迹结果;(F)蛋白质印迹结果的分析直方图。
论文链接:https://doi.org/10.1021/acs.biomac.2c00197
版权与免责声明:中国聚合物网原创文章。刊物或媒体如需转载,请联系邮箱:info@polymer.cn,并请注明出处。
(责任编辑:xu)
相关新闻
- 东华大学史向阳教授团队 Bioact. Mater.:全活性含磷树冠大分子纳米药物通过多靶点免疫调控与神经保护缓解缺血性脑卒中 2026-04-10
- 东华大学史向阳教授团队 AM:具有免疫调节功能的含磷树冠大分子载药纳米胶束通过协同调节多种免疫细胞增强肿瘤化学免疫治疗 2022-11-01
- 华南理工大学杜金志教授、都小姣教授 ACS Nano:可注射“特洛伊木马”水凝胶 - 释放可穿透免疫刺激纳米胶束用于胶质母细胞瘤术后治疗 2026-04-20
- 常州大学王建浩教授团队《Acta Biomater.》:药物储库型聚合物纳米胶束用于肿瘤长效治疗的研究成果 2025-07-08
- 法国CNRS彭玲团队 PNAS:纳米药物递送系统 - 自组装树形分子超分子纳米胶束通过劫持细胞外囊泡的方式深层递送抗癌药物 2023-06-07
- 中科大王育才/朱书/蒋为团队 Science:系统揭示高分子载体材料发生系统性清除的底层机制 2026-03-20
- 浙江大学王立教授、俞豪杰教授团队 JCIS:用于安全磁共振成像和刺激响应药物递送的纳米粒子 2025-09-09
