可视化观察大脑的自然状态是研究常见脑部疾病的重要方法。双光子荧光(2PF)显微成像因其激发波长在传统的近红外区(700-1000nm)和具有低的光漂白特性,通常被用于活体组织成像。然而,即使借助于颅窗,因激发光束在生物组织中的光散射,2PF成像技术也通常局限于浅层的生物组织成像。而且,由于失去了完整的颅骨,会导致术后动物存活率低。此外,对于大脑自然状态的干扰和脑组织的发炎是不可避免的破坏性干扰因素,会导致脑血管成像质量的降低。为了解决上述问题,三光子荧光(3PF)显微成像作为一种有效的成像方式正在迅速的发展。与传统的2PF成像方式不同,3PF成像利用近红外二区(NIR-II,1000-1700 nm)波段内的激发光和更高阶的非线性光学效应,这样能够显著的提高了穿透深度、时间和空间分辨和信号背景比(SBR)。尽管拥有这些优点,3PF成像的一个主要局限是缺乏具有大的三光子吸收截面和高荧光量子效率的有机染料。
聚集诱导发光(AIE)的纳米材料具有良好的抗光漂白性和生物兼容性等特点,近年来已有众多AIE发光材料被制备出来。然而,大多数的材料是基于四苯乙烯(TPE)的骨架,拥有相对复杂的分子结构,增加了AIE分子设计和化学合成的难度。因此,设计分子结构简单、易于合成的具有显著三光子荧光特性的高效AIE生物荧光探针,仍然是一个挑战。
近日,中山大学材料科学与工程学院梁国栋课题组与浙江大学光电学院钱骏教授课题组和香港科技大学唐本忠院士团队合作,设计并制备AIE荧光分子BTF。该AIE分子结构简单、合成简便,具有典型的AIE特性、高的固态荧光量子产率(42.6%)和深红/近红外(FR/NIR)荧光。合成的BTF分子能够通过纳米沉淀的方法,制备成AIE点。AIE点具有良好的生物相容性、大的Stokes位移、高的光稳定性和大的三光子吸收截面。BTF点作为有效的三光子荧光探针,可以对活体小鼠颅骨下血管进行三光子荧光成像。这是首次使用AIE点作为三光子荧光探针实现对完整颅骨下脑血栓过程的高穿透和高分辨的观测。
研究者设计的AIE染料BTF,它结构中有强电子供体三苯胺(TPA)、叔丁基(t-Bu)基团和电子受体富马腈(FN)。BTF具有典型的供体-受体(D-A)结构,使分子具有FR/NIR发射和显著的多光子吸收的能力。BTF可以溶解于常见有机溶剂中,但不溶于水。BTF在纯THF中发出微弱的荧光。当在BTF的THF溶液中加入少量水(fw≤50%)时,因为典型的扭曲分子内电荷转移(TICT)效应,BTF的发射红移,强度减弱。随着水含量的进一步增加(fw≥60%),BTF分子由于疏水作用而形成纳米聚集体,缓解了TICT效应,使AIE效应成为主导因素,导致BTF溶液的荧光强度增加。当溶液中fw = 90%时,光谱强度达到最大值,是纯THF溶液的5倍。因此,BTF是具有AIE特征的分子。
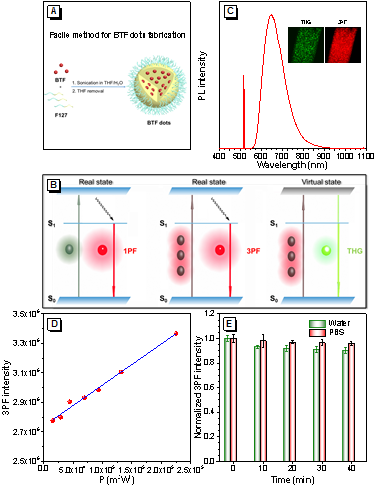
图1. A)双亲性聚合物F127包覆BTF分子形成BTF点的制备过程示意图。B)单光子荧光、三光子荧光和三次谐波产生过程示意图。C)1550 nm飞秒激光激发下BTF点的水相分散液的三光子荧光和三次谐波光谱。插图:毛细管内BTF点水中分散液的三次谐波和三光子荧光成像图。D)1550 nm飞秒激光激发下BTF点荧光强度和功率的依赖关系。E)1550 nm飞秒激光连续照射下不同时间点内的三光子荧光强度变化情况。
为了提高BTF分子在水中的分散性,使用双亲性聚合物F-127包覆形成BTF点(图1A),聚集态量子产率为36.1%。BTF点在1550 nm飞秒(fs)激光激发下能够激发出大约在650 nm处的三光子荧光和峰位在517 nm三次谐波信号(图1B、C)。值得注意的是,三光子荧光信号比三次谐波信号强,波长更长,更有利于体内深层组织成像(图1B)。通过测试,BTF的三光子吸收截面为2.56×10-79cm6s2。以1550 nm的激光连续照射40分钟, BTF点在磷酸盐缓冲液和水中的3PF强度保持在初始强度的90%以上(图1E),这种良好的光稳定性使得长时间的生物成像成为可能。
因为BTF点的良好的生物相容性特征,研究者研究了以BTF点作为3PF探针,小鼠开颅情况下的脑血管3PF成像。得到了900 μm的小鼠脑血管成像深度和三维高分辨率脑血管重构图。此外,还观察到在不同穿透深度产生的固有的三次谐波信号;并且三光子荧光信号与三次谐波信号良好匹配,可实现不同模式下的荧光成像,同时增加了生物成像的可信度。

图2. A-C)具有完整颅骨的小鼠脑血管的活体三维高分辨率图像,穿透深度为0至400 μm。D-F)沿(A)-(C)中黄线的横截面强度剖面图。脑血栓形成前(G,H)和后(I,J)脑血管的3PF图像。K)沿(G)和(I)中黄线的横截面强度剖面图。L)通过3PF显微成像技术,基于AIE点的完整颅骨脑血栓形成过程的可视化示意图。
基于3PF显微成像技术和BTF点本身的优势,研究者在活体穿颅情况下实现了小鼠脑血管成像,得到了0-400 μm成像深度的高分辨3PF成像图(图2A-C)。通过该图像,能够清晰的观测到小鼠脑部主要血管和微小毛细血管的空间网络结构。如图2D-F所示,标记的毛细血管的半高宽在200,300和400 μm深度分别为0.95,1.59和2.08 μm。脑血栓是一种常见的脑部疾病,可导致急性脑损伤甚至死亡。因此,研究者进一步利用BTF纳米点标记进行三光子荧光显微成像,用于监测完整颅骨小鼠的脑卒中过程。在大视场中可以观查到血栓形成前后脑血管内3PF信号的强烈变化(图2G-J)。通过对3PF图像中高亮线的定量分析,可以得出了同样的结论。在正常状态下,可以有效的监测到来自脑血管的高达92.1的强烈的3PF信号(图2H,K)。在小鼠脑中动脉堵塞形成后,由于血管缺血,在同一位置(图2J,K),3PF强度显著降低至1.1,已经与背景信号难以区分。而在相同成像条件下,对照组小鼠中未观测到脑血栓过程。因此,基于具有显著非线性光学效应的超亮AIE点,研究者首次实现了高对比度、非侵入性的观察完整颅骨的活体小鼠脑血栓的形成过程(图2L)。这项研究将会有助于开发新的高效非线性发光染料,用于非侵入性活体生物脑成像的研究。
以上研究成果以“Facile Synthesis of Efficient Luminogens with AIE Features for Three-Photon Fluorescence Imaging of Brain through Intact Skull”为题,近期发表在 Advanced Materials (Adv. Mater. 2020, 2000364) 上。中山大学秦玮研究员和浙江大学博士、新疆医科大学讲师努尔尼沙·阿力甫为论文的第一作者,梁国栋教授、钱骏教授和唐本忠院士为通讯作者。该项研究得到了国家自然科学基金、中央高校基本科研业务费专项资金、浙江省自然科学基金、香港研究资助局和创新科技署等的资金资助。
论文链接:https://www.onlinelibrary.wiley.com/doi/10.1002/adma.202000364
- 从“0到1”的飞跃 - 唐本忠院士团队《Acc. Chem. Res.》先驱报告:带你读懂聚集诱导发光(AIE)的前世今生 2026-03-23
- 南林蔡旭敏、港中深唐本忠/汪文锦团队 AFM: 松香基天然电子受体构建TICT活性的双功能BioAIE材料 2025-07-22
- 唐本忠教授/林荣业教授团队、胡连瑞研究员 Nat. Commun.:变色龙聚集诱导发光分子在光、热调控下六重稳定态的可控转换 2025-07-11
- 香港科技大学唐本忠教授团队 JACS:AIE-多酸晶体稳定自由基实现高效光热转化 2026-03-09
- 南林蔡旭敏/王石发、港中深唐本忠、浙大张鉴予 Chem. Sci.:从天然电子受体到极性/多晶型响应的BioAIE智能防伪材料 2025-12-17
- 港中大(深圳)唐本忠教授、赵征教授/港科大林荣业教授团队 Matter: 基于立体异构AIEgens在动态信息防伪与加密的应用 2025-07-28
