肝纤维化是一种伴随所有形式的慢性肝病产生的病理特征,表现为肝脏中过度沉积的细胞外基质(extracellular matrix, ECM)。目前的研究已经证实了肝纤维化的可逆性,对肝纤维化进行及时有效的干预治疗,能减少向肝功能衰竭、肝硬化和肝癌的恶化进展,具有重大意义。并且已有许多药物表现出潜在的抗纤维化活性,然而由于药物本身的溶解性、靶向性等因素,其体内功效和安全性受到限制。肝星状细胞(hepatic stellate cell, HSCs)是存在于肝窦Disse空间的一种贮留非实质细胞,是肝纤维化时细胞外基质的主要来源,对于肝纤维化发生发展至关重要。因此,靶向HSCs的高效纳米药物递送系统一直是抗肝纤维化治疗的研究热点。课题组在前期的研究工作中探索了靶向HSCs的化学/基因药物疗法(chemogene therapy)协同治疗肝纤维化(J. Control. Release 2018, 283, 113)。随着研究,课题组发现在Disse空间中过度沉积的纤维化基质(主要是I型胶原蛋白),也会作为一种递送屏障,严重阻碍纳米制剂向HSCs的有效递送。
针对这一问题,中国药科大学姜虎林教授课题组在本研究中报道了一种具有基质渗透性和HSCs靶向性的双重功能的 “nanodrill”纳米递送系统(CRM/NIL)。该体系通过对聚合物纳米粒(PLGA-PEG)进行修饰,引入I型胶原酶(Collagenase I)和视黄醇(Retinol)。到达肝窦后,遇到I型胶原蛋白屏障,纳米载体CRM表面修饰的I型胶原酶能有效降解细胞周围过度沉积的胶原蛋白,从而促进它们在细胞外基质中的渗透;随后,表面修饰的视黄醇可以促进CRM进一步有效识别并靶向HSCs;最终,实现HSCs的高效靶向、增强摄取。
这项工作表明具有双重功能的CRM是肝纤维化药物递送的有效载体,并且首次证明了修饰I型胶原酶可以促进纳米载体在纤维化肝脏中的渗透和蓄积,是构建更高效的靶向HSCs纳米药物递送系统的新策略。
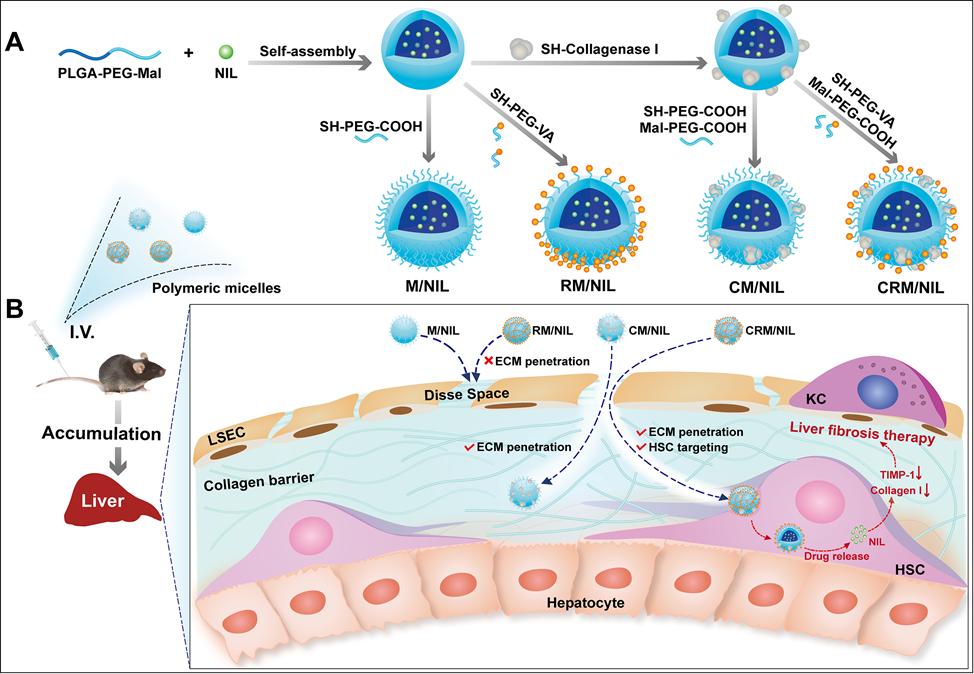
(A)聚合物胶束制备示意图,(B)聚合物胶束体内过程示意图。
以上相关研究成果以“Extracellular matrix-penetrating nanodrill micelles for liver fibrosis therapy”为题发表在国际期刊《Biomaterials》(IF:10.273)上。课题组成员硕士毕业生范倩倩和硕士研究生张程璐为共同第一作者。
- 河北工大邢成芬课题组《Nano Lett.》:基于近红外光响应共轭聚合物纳米粒子的免疫激活抗真菌策略 2022-12-27
- 上海中医药大学冯年平教授课题组 CEJ:多功能多臂聚合物纳米粒联合新型可溶性微针的一体化递药策略用于关节炎的治疗 2021-12-22
- 浙工大高从堦院士团队与北工大安全福教授团队合作《Adv. Mater.》:MOFs强化两性聚合物纳米流体膜 2021-08-26
- 中国海大何治宇/于良民 Adv. Sci.:基于传统中药冰片的聚合物胶束脑内药物递送系统-用于精确适应病理机制的缺血性脑卒中治疗 2025-01-21
- 复旦大学占昌友教授团队《Nano Today》:亲和诱捕法实现生物介质中PEG化聚合物胶束的高效分离-破译聚合物胶束的体内命运 2024-04-25
- 国科大屈小中教授课题组 Angew:在高分子-蛋白多层次结构纳米组装体制备和应用研究中取得进展 2024-02-27
