微/纳米颗粒在催化、传感器、涂料、复合材料、光电、能源、环境和生物医学等领域均有广泛和重要的应用价值。颗粒的表面化学和物理结构决定了胶体粒子的稳定性、生物活性和相容性等关键参数。因此,颗粒表面工程已成为材料设计和应用的一个重要领域。目前能在温和水溶液中一步、低成本实现对具有不同成分、大小、形状和结构的微纳米颗粒的表面功能化的普适性方法很少。
生物大分子如多肽和蛋白质以β-sheet折叠结构为核心而形成的淀粉样积聚体(amyloid)是存在于自然界的一类重要的生物高分子组装结构。研究表明其除与多种神经退行性疾病如阿尔茨海默、帕金森症等有重要关系之外,还有一大类amyloid组装体不仅没有生物毒性,而且可以作为崭新的功能性生物材料而应用于包括生物医药、先进材料制造在内的诸多高技术领域。事实上,自然界常使用诸多的amyloid结构和相应的材料来实现一系列无关疾病的有益生物功能,如结构材料、信息传导、催化载体和蛋白质储藏等。此类amyloid材料表现出优异的生物相容性、高的力学性能、丰富的界面功能基团和组装形态,从而有望在组织工程、药物缓释、生物传感器、模板导向纳米材料合成、膜材料、(有机/无机杂化)复合材料、光电材料、仿生黏附等领域产生重要影响。
相转变溶菌酶(phase-transited lysozyme,PTL)最早由杨鹏教授课题组于2016年提出(Adv. Mater. 2016, 28, 7414),是一类区别于传统淀粉样蛋白质积聚的新的类淀粉样蛋白质组装体系。其特点在于组装条件温和可控、速度快、材料和过程成本极大降低。目前此体系至少包括两种新颖结构即纤维网络和纳米薄膜,均可在各类宏观材料表界面实现稳定粘附和改性。该体系不仅适用于溶菌酶,而且可拓展到其他蛋白质中,如牛血清白蛋白 (BSA)、α-乳白蛋白 (α-Lactalbumin)、胰岛素 (insulin)等。其能发生此类组装的共性规律是其蛋白质一级结构中存在能发生淀粉样积聚的高纤维化可能性序列结构,同时其二级结构中大量存在由分子内二硫键锁冻结的α-螺旋结构。在此分子基础之上,加入高效二硫键还原剂Tris(2-carboxyethyl)phosphine (TCEP)可快速打开分子内二硫键而解锁α-螺旋结构,诱导其向更加低能量的β-sheet自发转变而形成类淀粉样组装体。在系统探讨了其组装机理(Angew. Chem. Int. Ed. 2017, 56, 13440; Biomater. Sci. 2018, 6, 836)、界面粘附机理(Colloid Interface Sci. Commun. 2018, 22, 42)和应用基础(Adv. Mater. 2016, 28, 579; Adv. Funct. Mater. 2018, 28, 1704476; Angew. Chem. Int. Ed. 2017, 56, 9331; Macromol. Biosci. 2012, 12, 1053)之后,日前杨鹏教授课题组进一步将该方法拓展到微纳米颗粒表界面(图1),从而提供了一种简单、快速、低成本、生物相容的蛋白质涂层,可在金属、无机、聚合物和活细胞等微纳米颗粒上成功粘附。
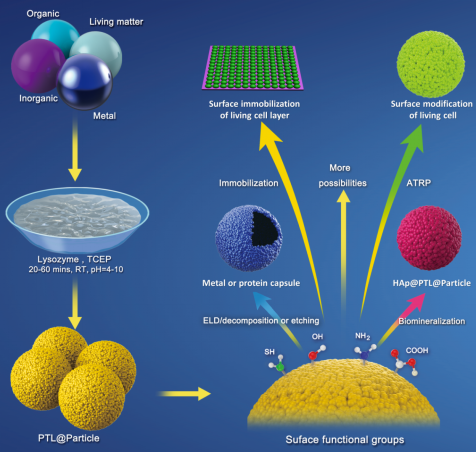
图1. 基于PTL方法的微/纳米颗粒表面改性及工程化应用示意图。
该策略支持了微纳米颗粒丰富可调的表界面工程之应用:
1. 该涂层表面具有丰富的官能团(如羟基、羧基、氨基、巯基、胍基等),可通过多重键合机理而在各种成分的微纳米颗粒表面形成粘附牢固的PTL涂层(可抵御超声、极端酸碱pH和有机溶剂的剥离);并为后续的功能化提供了可调的反应位点(如可引发表面活性接枝聚合、仿生矿化、无电沉积等)(图2,3)。

图2. 在聚合物(聚苯乙烯,PS)以及无机(二氧化硅,SiO2)微纳米颗粒表面涂覆PTL层的过程及电镜表征。
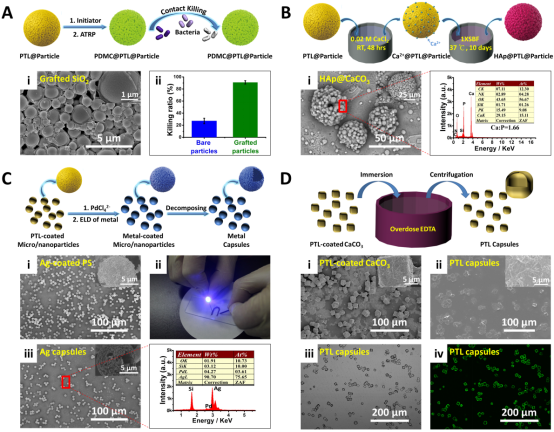
图3. PTL涂层支持的微/纳米颗粒表面功能化。(A) 通过原子转移自由基聚合(ATRP)在PTL涂覆的SiO2颗粒表面接枝具有抗菌功能的聚甲基丙烯酰氧乙基三甲基氯化铵 (PDMC)聚合物刷;(B) 通过界面仿生矿化在PTL涂覆的CaCO3粒子表面生长羟基磷灰石 (HAp);(C) 通过钯催化的无电沉积在PTL涂覆的PS颗粒上沉积高导电性金属层以及通过去除PS模板制备空心金属胶囊;(D) 通过ethylenediaminetetraacetic acid disodium salt (EDTA)蚀刻去除CaCO3模板的方法制备空心蛋白质胶囊(即壳层为纯的PTL膜)。
2. 可利用该策略简便、高效的制备Janus颗粒及其在表面的微阵列排布。
3. 可利用该策略批量制备以有机聚合物为核的高导电性金属微纳米颗粒、以及蛋白质或金属为壳的空心胶囊。
4. 可直接利用该策略对活细胞表面进行包覆及进一步的化学改性(如从活细胞表面引发活性接枝聚合),从而实现对活细胞的功能调控和在固体表面的活细胞层固定。如可将该涂层包裹在酵母菌上,从而提高其机械稳定性和抵抗外界有毒物质(如溶细胞酶)的攻击。在不显著影响其活性的前提下,通过PTL涂层介导的表面粘附可将一整层酵母细胞稳定固定在基材上,为后续的细胞工厂、细胞/器官芯片和固定化生物反应器之应用提供了潜在支持(图4)。

图4. PTL封装酵母细胞以实现对其保护、表面功能化和表面固定等多种用途。(A) 空白酵母细胞和PTL包裹的酵母细胞对比;(B) 在不同缓冲液中培养出的酵母活性对比;(C) PTL包裹的酵母细胞对外界有毒物质(溶细胞酶,Zymolyase)的抵抗示意图及在溶细胞酶存在下的抵御能力测试;(D) 评价PTL膜阻隔溶细胞酶能力的Zymolyase透过性测试;(E) 用PTL方法将活酵母层固定在硅片上并代谢葡萄糖的反应过程前后对比;(F) 循环使用固定化酵母层代谢葡萄糖的反应活性测试;(G, H) 通过表面引发ATRP法在PTL包裹的酵母细胞表面接枝聚乙二醇甲基丙烯酸酯 (PEGMC)聚合物刷。
以上工作在线发表在材料学权威期刊Adv. Mater.(先进材料)上。
该论文第一作者为硕士生刘瑞瑞,通讯作者是杨鹏教授。合作单位包括天津医科大学口腔医学院张旭教授课题组。该课题得到了国家自然科学基金委 (No. 51673112, 51303100) 等项目的资助。
论文链接:https://onlinelibrary.wiley.com/doi/full/10.1002/adma.201802851
杨鹏教授课题组简介:

陕西师范大学化学化工学院杨鹏教授课题组组建于2012年底,隶属于应用表面与胶体化学教育部重点实验室。主要致力于基于蛋白质类淀粉样组装的多功能仿生界面材料基础和应用研究。经过六年的努力,已取得了一定的系统性研究成果,已在Macromol. Biosci. (2012, 12, 1053)、Chem. Rev. (2013, 113, 5547)、Adv. Mater. (2016, 28, 579, VIP paper)、Adv. Mater. (2016, 28, 7414, Frontispiece)、Angew. Chem. Int. Ed. (2017, 56, 9331, Hot paper)、Angew. Chem. Int. Ed (2017, 56, 13440)、Adv. Funct. Mater. (2018, 28, 1704476) 、Adv. Mater. (2018, 1802851)等权威期刊发表综述和研究论文二十余篇。
