近日,中国科学院深圳先进技术研究院劳特伯医学成像中心分子影像团队与新加坡国立大学刘斌教授合作,构建了近红外二区(1000-1700 nm)聚集诱导发光(AIE)分子,通过纳米共沉淀技术制备了RGD多肽靶向的AIE探针,实现了脑胶质瘤的近红外二区荧光/近红外一区光声双模态分子成像。研究成果Bright Aggregation‐Induced‐Emission Dots for Targeted Synergetic NIR‐II Fluorescence and NIR‐I Photoacoustic Imaging of Orthotopic Brain Tumors(明亮的聚焦诱导发光点用于原位脑肿瘤的近红外二区荧光/近红外一区光声协同靶向分子成像)在线发表在Advanced Materials(IF=19.791)杂志上。
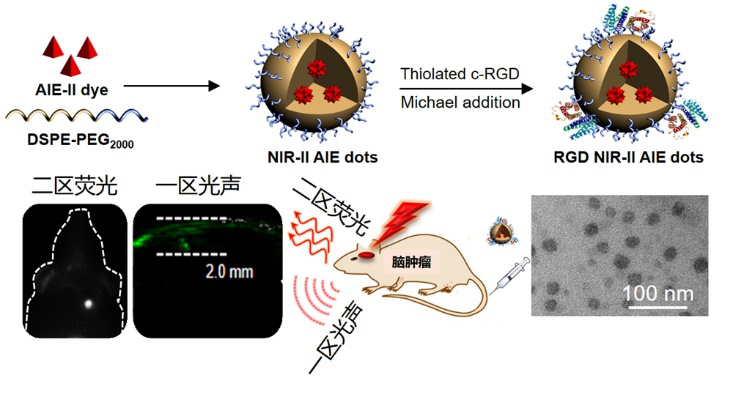
图 近红外二区AIE探针用于脑胶质瘤的荧光/光声双模态分子成像
近红外二区(NIR-II,1000~1700 nm)荧光成像是近年来发展起来的一种新型成像技术。与传统的可见光(400-700 nm)和近红外一区(NIR-I, 700-1000 nm)荧光成像相比,光子在 NIR-II表现出更高的穿透能力、更低的组织吸收和散射。利用 NIR-II 荧光成像技术可实现高灵敏(皮摩尔~纳摩尔)、高分辨(~微米级)、超快速(~毫秒级)的成像。
在科技部973项目“脑胶质瘤精准诊疗技术的关键科学问题研究”的资助下,郑海荣、盛宗海和刘斌等在前期工作的基础上(ACS Nano 2017, Materials Horizons 2017, Advanced Functional Materials 2016, ACS Nano 2014),针对现有NIR-II荧光探针量子产率低(<1%),聚集诱导荧光淬灭的瓶颈问题,设计制备了高量子产率的(6.2%)NIR-II聚集诱导发光(AIE)探针,在小鼠原位脑胶质瘤模型上,实现了高分辨(38微米)、高信背比(S/N=4.4)的NIR-II荧光和穿颅骨的NIR-I光声协同靶向双模态分子成像,为成像引导脑胶质瘤精准手术提供了一种全新的方法和技术。
该项目得到国家973计划、国家自然科学基金、广东省磁共振成像与多模系统重点实验室等基金支持。
论文链接:https://onlinelibrary.wiley.com/doi/abs/10.1002/adma.201800766
- 从“0到1”的飞跃 - 唐本忠院士团队《Acc. Chem. Res.》先驱报告:带你读懂聚集诱导发光(AIE)的前世今生 2026-03-23
- 南林蔡旭敏、港中深唐本忠/汪文锦团队 AFM: 松香基天然电子受体构建TICT活性的双功能BioAIE材料 2025-07-22
- 唐本忠教授/林荣业教授团队、胡连瑞研究员 Nat. Commun.:变色龙聚集诱导发光分子在光、热调控下六重稳定态的可控转换 2025-07-11
- 杭师大黄又举/丁彩萍团队 ACS Nano:铂基超晶格生物探针赋予生物传感器“阈值特异性”实现结核性脑膜炎准确评估 2026-02-10
- 杭师大黄又举教授团队 AFM:超强H2O2亲和力的体外医疗诊断试剂盒 2025-09-08
- 北京大学邵元龙《Adv. Mater.》综述:用于组织电子设备接口的生物材料基纤维状植入式探针 2025-06-27
