大豆分离蛋白质在二甲亚砜/尿素中溶解特性的研究
时间:2005-05-27
肖茹 尹端 顾利霞
纤维材料改性国家重点实验室 东华大学 上海 200051
石油基材料由于具有高强、质轻和价低等优良的性能,是现代社会最重要的材料之一。如何处理废弃的不能降解石油基材料成了一大难题。而且石油资源是有限的,因此来源丰富可生物降解的天然大分子引起材料科学家的重视。大豆蛋白质是其中较为突出的一种材料。
在大豆分离蛋白质的提取和其作为材料的理化性能研究中不可避免地会涉及溶解,大豆蛋白质在碱溶液中的溶解已有大量的文献报导[1-2],华欲飞等人研究了大豆蛋白质在乙醇水溶液中的理化特性[3],蛋白质是一种极性物质,Kikkoman研究了大豆蛋白质在一系列有机溶剂中的变性溶解情况,发现它在非极性溶剂如苯、甲苯、乙烷、四氯化碳中几乎不溶[4]。但未见采用二甲亚砜/尿素作为大豆蛋白质的混合溶剂[5]。本文根据文献自制了7S球蛋白、11S球蛋白及大豆混合蛋白,研究了尿素浓度、溶解时间、溶解温度对大豆蛋白质溶液特性粘度、紫外吸光度、流体力学半径、电导率的影响。
实验方法
将大豆蛋白质(分别为7S球蛋白、11S球蛋白、大豆混合蛋白)、尿素、二甲亚砜按蛋白质含量为二甲亚砜的0.1wt%,尿素浓度分别为二甲亚砜的0、1、2、3、4、5mol/l的比例混合。30℃水浴开始加热,升温速率1℃/min,当水浴温度升至溶解温度(80、85、90、95、100℃)后开始恒温计时,达到溶解时间(0、1、2、3、4小时)后取样。
结果与讨论
图1和图2分别是大豆蛋白质溶液在尿素浓度为0M、1M、2M、3M、4M、5M,溶解温度为90℃,溶解时间为2h时的特性粘度和流体力学半径。由图可知:随着尿素浓度增大,蛋白质溶液特性粘度、流体力学半径均有显著提高。
这是由于大豆蛋白质的天然结构中,亲水基团倾向位于高级结构外部,疏水基团则倾向位于蛋白质分子的内核。因此当大豆蛋白质的处于水溶液中,依靠多肽链中亲水基团与水分子形成氢键而实现蛋白质外壳水化。当采用DMSO为溶剂时,由于DMSO分子较大且具有两个非极性头,空间位阻效应较大影响了形成氢键的能力,因此蛋白质外壳并不能被充分溶剂化。加入变性剂尿素后,由于尿素分子中的氢原子与肽链中的氧原子相作用而形成氢键,这样使肽链自身可形成的氢键减少,使多肽分子中靠氢键维系的二级结构如螺旋、折叠、自由回转结构遭到破坏,使大豆蛋白分子伸展变性溶解。
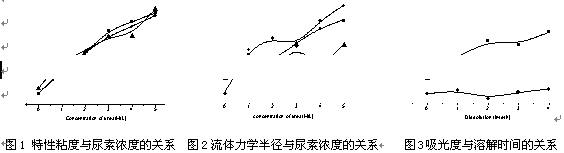
由图3可知:随着溶解时间的延长,7S球蛋白溶液的峰值有一个逐渐增大的趋势,这说明时间有助于7S球蛋白的溶解;11S球蛋白溶液峰值的变化很小,基本趋于水平;而大豆混合蛋白由于含有7S球蛋白和11S球蛋白,所以它的峰值变化结合了上述两种蛋白质的趋势,随着溶解时间的延长缓慢上升。
图4电导率与溶解温度的关系由图4可知:升高温度,三种蛋白溶液的电导率都增大了。这说明随着溶解温度的升高,蛋白质分子肽链中氨基酸残基上的各种极性基团解离出来,即使蛋白质分子降解了,极性基团依然存在,依然会解离出来,所以导致溶液的电导率一直上升。

结 论
1.尿素加入是引起大豆分离蛋白质变性溶解的主要原因;体系中尿素浓度越大,处理温度越高,处理时间越长,越有利于破坏大豆分离蛋白质氢键、疏水作用等空间作用力,促其溶解。但温度过高,时间过长,大豆蛋白质易于降解。
2.确定了尿素浓度:2M,溶解温度:90℃,溶解时间:2h,为体系的较佳溶解条件。
3.温度、时间、尿素浓度对7S球蛋白、11S球蛋白和大豆混合蛋白溶解的影响基本一致。
参考文献
[1] Kelley J.J., Pressey Russell. Cereal Chemistry, 1966,43:195-206
[2] Nir I., Feldman Y., Aserin A., Garti N.. Journal of food science,1994,59:606-610
[3] 华欲飞、谷文英、沈培英等.无锡轻工大学学报,1996,15(2):129-134
[4] Kikkoman. Cereal Chemistry,1969,46:156-163
[5] Setsuko Iwabuchi, Fumio Yamauchi. J. Agric Food Chem., 1987,35: 200-205

