凝聚体由于具有组装简单以及良好的生物相容性等优势,作为一种新型药物载体引起了广泛关注。然而,凝聚体的不稳定性限制了其在药物递送中的应用。例如,基于静电相互作用的传统凝聚体容易受到pH/盐的影响发生解离,而基于氢键的凝聚体容易发生聚并,从纳/微米颗粒变为密集相。近日,山东大学研究团队提出了一种交联多酚-聚乙二醇(PEG)凝聚体制备PEG纳米颗粒(PEG NPs)的简单方法(图1),该方法避免了传统模板法中的模板去除过程,制备的PEG NPs在生理环境中表现出良好的稳定性,在生物医学应用中具有重要的潜在价值。相关研究成果“Coacervate-Derived Assembly of Poly(ethylene glycol) Nanoparticles for Combinational Tumor Therapy”发表在Advanced Healthcare Materials上。山东大学化学与化工学院崔基炜教授为该论文的通讯作者,山东大学博士生刘含茹为该论文的第一作者。
在本工作中,作者通过理论模拟等方法证明了氢键是该凝聚体形成的主要驱动力(图2)。该方法适用于各种多酚(例如单宁酸、EGCG、原花青素和丹参酚酸B)和交联策略(例如,巯基-二硫键交换、点击化学和席夫碱反应)(图3)。此外,PEG NPs中多酚的存在有助于负载金属离子(即Ru、Gd、Mn、Fe)和药物(即DOX)用于肿瘤成像和联合肿瘤治疗。具体来说,Gd@PEG和Ru@PEG NPs在磁共振成像和光热成像中表现出优异的性能。DOX&Ru@PEG NPs可通过联合光热治疗和化疗显著抑制肿瘤的生长,表现出对肿瘤抑制的协同作用(图4)。这种基于动态共价交联稳定凝聚体的方法为开发凝聚体衍生的药物递送系统提供了新策略。
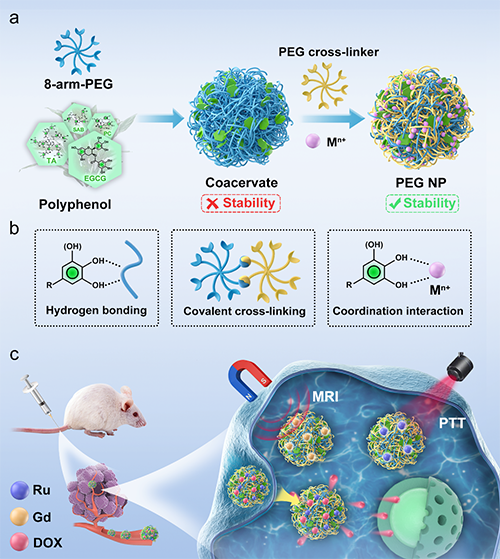
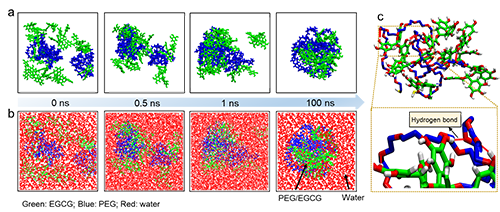
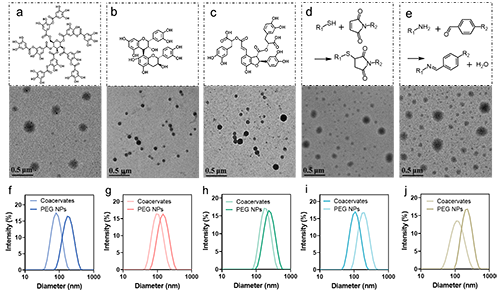

图4 凝聚体衍生的PEG NPs在肿瘤成像以及肿瘤治疗中的应用。
Coacervate-Derived Assembly of Poly(ethyleneglycol) Nanoparticles for Combinational Tumor TherapyHanru Liu, Dandan Ren, Huimin Geng, Yuan Tian, Mengqi Li, Ning Wang, Shiling Yuan, Jingcheng Hao, and Jiwei Cui*Adv. Healthcare Mater. 2025, 2403865.
文章链接:https://onlinelibrary.wiley.com/doi/10.1002/adhm.202403865
- 华南理工边黎明、赵鹏超、张琨雨教授团队 Nat. Chem.:开发超强水下“万能胶” - 灵感源自海洋生物 2026-03-31
- 西湖大学王怀民团队《Adv. Mater.》:利用化学策略在活细胞中构建人工生物聚集体方面取得重要进展 2021-10-12
- 中科院上海光机所: 原子芯片上的玻色-爱因斯坦凝聚体在我国诞生 2008-12-03
- 山东大学崔基炜教授团队 ACS Nano: 硬度可调的聚乙二醇纳米颗粒调节纳米-生物相互作用,增强靶向药物递送 2025-06-12
- 华南理工大学杜金志教授、都小姣教授 ACS Nano:可注射“特洛伊木马”水凝胶 - 释放可穿透免疫刺激纳米胶束用于胶质母细胞瘤术后治疗 2026-04-20
- 西安交大吴道澄团队 ACS Nano:分子堆砌@无限配位聚合物复合纳米粒实现肿瘤连续高强度光热-热动力交替循环治疗和化疗 2025-08-01
- 巴黎高科化学学院李敏慧教授与合作者 JACS: 创新型“类酶”纳米材料 → 饿死癌细胞 2025-07-20
