随着人口老龄化的加剧,延缓衰老成为急需解决的重大问题。睾酮的缺乏在男性中老年群体中越来越常见,睾酮作为男性个体最重要的性激素,睾酮缺乏会影响睾丸功能,而且伴随着性功能障碍、脂肪堆积、 骨质疏松、肌肉萎缩、认知障碍等并发症,进一步加剧全身衰老。目前的临床治疗手段仍局限于外源性的睾酮补充,这种疗法有许多副作用,如红细胞增多,肝功能受损,前列腺增生,严重会破坏下丘脑-垂体-性腺的 (HPG) 轴的调节,导致睾丸精子发生和内分泌功能减退。因此亟待寻求一种更安全、有效、且持久的治疗方式,用于治疗睾酮缺乏症,提升男性生活质量和幸福感。
近日, 华南理工大学材料科学与工程学院施雪涛教授团队在国际期刊Advance Science发表“ Reconstructing the Stem Leydig Cell Niche via the Testicular Extracellular Matrix for the Treatment of Testicular Leydig Cell Dysfunction ”的最新论著。这项工作研发了一种可塑性、温敏性和可注射性的睾丸脱细胞外基质水凝胶 (TdEC),联合睾丸间质干细胞 (SLC) 治疗睾酮缺乏综合征。SLC是间质细胞 (LC) 前体细胞,可以增殖分化为LC,产生睾酮。研究发现衰老的睾丸间质微环境会导致SLC的增殖和分化为LC的能力下降。脱细胞外基质既是结构支持的力学支架,又是细胞生长和信号传导的功能基质,是一种具备良好的生物相容的材料。该工作对现存的组织脱细胞方法做了针对睾丸组织的特异性优化,成功制备了睾丸组织TdECM。对脱细胞前后的组织学染色和Elisa检测证明细胞被有效清除,同时保留了细胞外基质的基底结构。SEM表征了水凝胶的胶原纤维的表观形貌,蛋白组学分析进一步解析了睾丸脱细胞外基质的主要成分组成和相关的信号表达。体外的细胞实验及免疫荧光、qPCR和RNA转录组测序证明TdECM能够有效促进SLC增殖和分化为LC,从而显著提升睾酮的分泌水平。

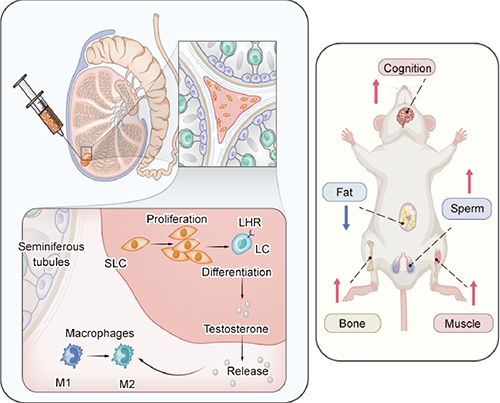
本研究针对男性睾酮缺乏症,开发了TdECM-SLC的组织工程治疗体系,通过原位注射TdECM-SLC,显著提升了睾酮缺乏症个体的血清睾酮水平,从而改善了睾酮缺乏的全身症状,这种原位注射细胞外基质包裹干细胞的治疗手段具备效果显著、持续时间长、不破坏HPG轴的调节机制等优势,为临床的睾酮缺乏症的治疗提供了一种前瞻性的方案,具有重要的研究价值和广阔的应用前景。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/advs.202410808
- 暂无相关新闻
