微针经皮给药是一种非侵入性技术,通过穿透角质层,将微量药物递送至皮肤及循环系统。这种技术增强了药物的吸收与生物利用度,降低了所需剂量,同时赋予微针持续释放的特性,提供稳定的治疗效果。然而,目前广泛应用的可溶解型微针在药物释放后缺乏对深度和扩散范围的精确控制,尤其在厚皮肤或深层组织中限制了其应用。研究者们正致力于实现药物释放的精确控制,探索如磁场和光基控制等外部方法,但这些方法常需复杂设备,增加了使用难度和成本。一些研究者还试图通过靶向模块改进药物扩散方向,但这可能增加安全隐患并阻碍应用。近年来,气体疗法引起关注,通过气体驱动药物释放,提供了一种创新的方法。然而,现有的气体生成材料在反应条件和持续性上存在限制。
近期,天津医科大学生物医学工程与技术学院/天津大学医学院郑斌团队开发了一种微生物驱动的气动微针给药系统,利用封装的产气微生物(如肠杆菌ATCC 13048)持续产生氢气,提供药物深层渗透的推进力。这种创新结合了微生物的产气机制与经皮药物释放,能够主动将药物推送到更深层组织,有效克服皮肤阻力,从而实现药物的深层扩散。在银屑病的治疗中,过度增殖的角质形成细胞是导致表皮增厚的主要原因。他们的微生物驱动微针技术通过在微针内封装产气微生物,持续产生气体,从而推动药物深入增厚的表皮,直接靶向过度增殖的细胞。这不仅抑制了异常增殖,还减少了炎症,显著改善了银屑病症状。此技术为微针给药提供了创新解决方案,实现了按需和可控的药物递送。
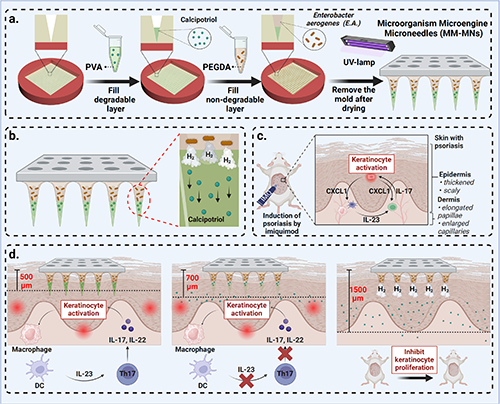
微生物作为气动力源的潜力
肠杆菌(E.A.)作为一种常见的肠道微生物,能够有效发酵多种糖类(如葡萄糖、乳糖和蔗糖)并持续产生气体,主要生成氢气(H?)。研究表明,E.A.的气体生产与底物浓度、培养时间和接种量密切相关。通过气相色谱分析,E.A.在适宜条件下(如20 mg/mL的葡萄糖浓度)可在12小时内产生高达28.7 mL的气体,最大气体生产速率达到1.65 mL/s。为了展示其作为微生物微发动机的潜力,实验中通过琼脂试管观察到,E.A.可推动琼脂达到最大位移12 mm,显示出约0.04 N的推进力。这些结果为E.A.在动态气体疗法中的应用提供了基础,表明其有潜力作为气动力源。
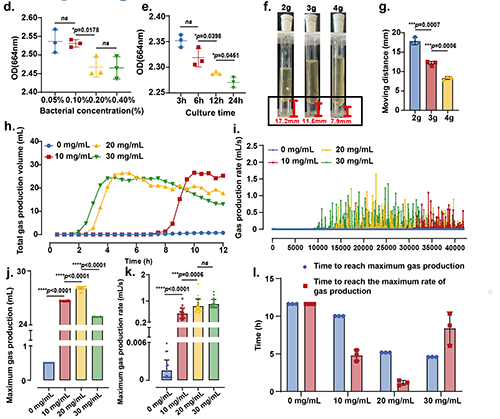
图2 微生物有潜力作为气动力的来源
微生物微发动机微针的制备与验证
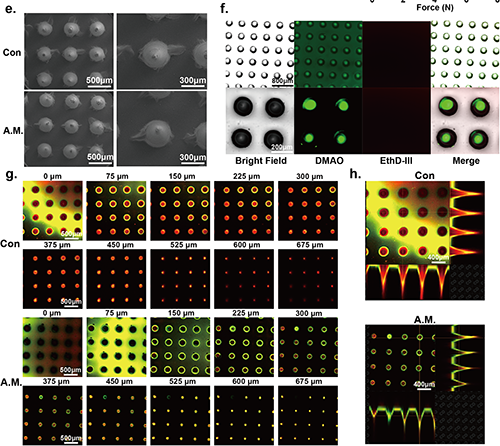
图3 微生物微引擎微针(MM-MNs)的制备和细菌活性验证
微生物微发动机微针(MM-MNs)气体穿透深度与药物释放性能的表征
为了确保微生物微发动机微针(MM-MNs)的有效功能,必须定量评估其气体生产能力及持续时间。研究表明,通过调整微针中加载的葡萄糖浓度,可以有效控制气体的生成。实验中制备了不同浓度的微针,结果显示30 mg/mL葡萄糖的微针具备最长的气体生产持续时间及最大气体产量。此外,MM-MNs的气体穿透能力通过插入猪皮进行测试,结果显示在不同厚度的皮肤中,气体渗透能力保持良好,特别是在5 mm厚度时仍能有效渗透。这为微针在推动药物进入组织方面提供了重要基础。综合数据表明,E.A.所产生的气体能够渗透至真皮层,最大渗透深度超过5 mm,展示了其作为气动马达在药物递送中的巨大潜力。
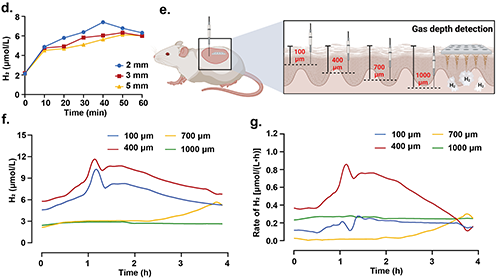
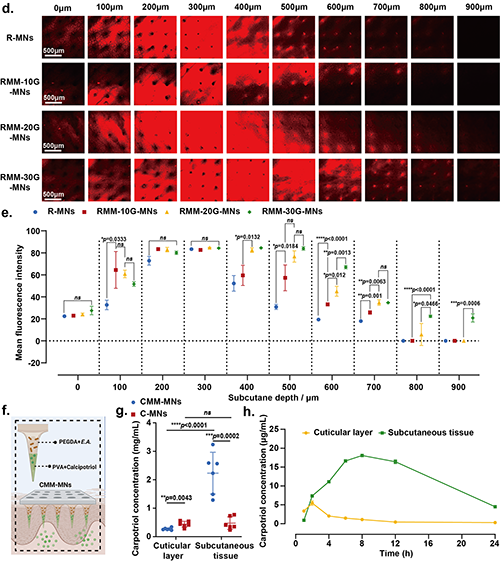
图5 微生物微引擎微针(MM-MNs)药物输送性能的表征。
药物在皮下的扩散受微生物发动机的气体产生行为控制
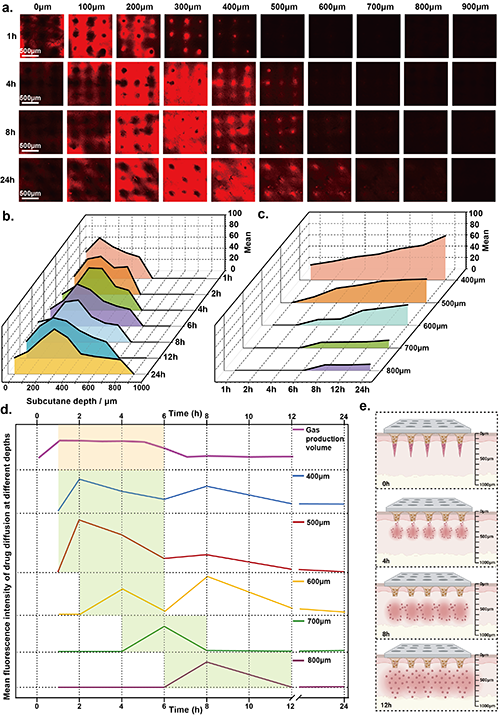
图6 药物在皮下的扩散受微生物引擎产生气体行为的控制。
使用微生物微发动机微针(MM-MNs)治疗牛皮癣
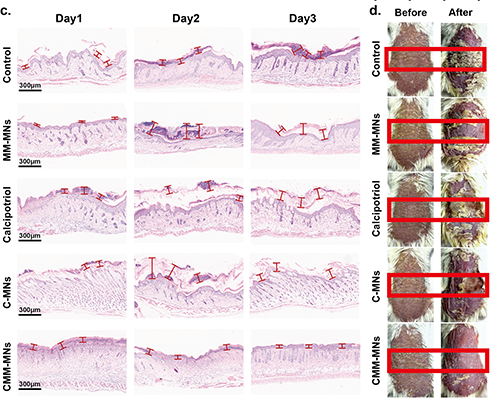
图7 微生物微引擎微针(MM-MNs)对慢性银屑病治疗的疗效。
总结
该研究提出了一种具有可调推进力的活体微针微引擎系统,利用内部加载的产气微生物实现气体动力学的驱动。这种系统显著增强了微针在皮肤下的药物溶解与释放能力,提高了透皮给药的深度和扩散效率。所开发的微针基质由PEGDA制成,包裹肠杆菌(E.A.),展现出超越传统金属基材的优越特性。微生物的持续气体产生可施加超过0.04 N的推动力,使药物深度可达1000 μm,较传统微针提高200%以上的输送效率。此外,微针中微生物的隔离设计有效防止了组织损伤,保证了生物相容性。在牛皮癣小鼠模型中,该系统通过输送卡泊三醇显著改善了症状,显示出其在治疗深层组织病变方面的潜力。气体在皮肤微环境中的扩散和压力分布是药物输送的关键因素。实验发现,气体在皮肤中的扩散表现出显著的横向和纵向特性,形成的局部高压环境有助于药物向深层扩散。通过调节微针中葡萄糖浓度,可以控制气体的释放速度和药物的扩散范围。未来研究应着重于微针孔中气体扩散的物理模型及其对药物输送的影响,尤其是高分子量药物的传输效率。此外,探索不同类型的微生物及其气体成分的潜在疗效,将进一步拓展该技术的应用范围。通过设计环境响应的活微生物气动微针,结合疾病特异性因素,进一步增强其药物释放的可控性和效率,从而提供一种创新的药物输送策略。
论文链接:https://www.nature.com/articles/s41467-024-53280-8
