心脏起搏器作为植入式医疗电子器械的代表,能够有效治疗心律失常疾病。然而,心脏起搏器的电池续航能力有限,许多患者一生需更换多个起搏器,这无疑会增加患者的医疗负担和手术并发症风险。此外,传统有导线起搏器在临床实际应用中会引起导线磨损及断裂、起搏器囊袋破溃和感染、穿刺血管的血栓与堵塞及疤痕局部疼痛等问题。如何提升心脏起搏器的服役时间协同实现无导线电刺激新模式一直是医疗电子器械领域研究的热点和难点。

近日,中国科学院北京纳米能源与系统研究所李舟研究员团队,与国家心血管中心/阜外医院华伟主任、北京航空航天大学刘卓副教授、杭州电子科技大学王宁宁教授等研究团队联合在Nature Communications杂志在线发表了题为“A self-powered intracardiac pacemaker in swine model”的最新研究成果,介绍了一种新型自供能心腔内起搏器。 该研究团队围绕临床疾病诊疗,一直聚焦基于纳米发电机技术的自供能医疗电子器械的研究和开发。早在2006年,王中林院士首次在美国《科学》杂志(Science)上提出了纳米发电机的概念(Science, 2006, 312(5771): 242-246)-单根氧化锌纳米线将机械能转化为电能。自此,李舟研究员就开始尝试通过纳米发电机技术从生物体的运动中收集机械能并转化为电能。2010年,成功研制了基于氧化锌纳米线的植入式压电纳米发电机,并成功收集了大鼠的心跳能量(Advanced Materials, 2010, 22(23): 2534-2537)。该纳米发电机的输出电压和电流只有1 mV和1 pA,如何获得更高的能量输出?如何利用这些微小的能量驱动医疗电子器件?是要继续攻克和解决的问题。

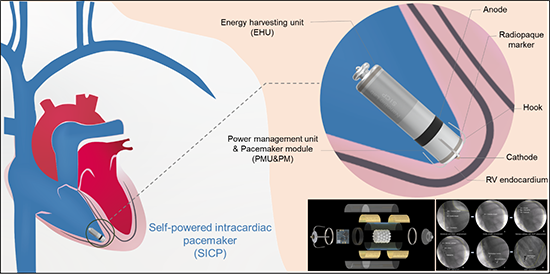
2019年至今,研究团队围绕器件材料优化,结构设计,系统集成加工和大动物实验评估,基于摩擦起电和静电感应耦合效应研制了一款胶囊形状的自供能心腔内无导线起搏器(self-powered intracardiac pacemaker, SICP)。项目团队同时开发了具有能量存储功能和电脉冲发送功能的微型低功耗起搏芯片(0.5 ms/1.5 V),以及与SICP尺寸匹配的心脏内固定装置/介入递送系统。该起搏器的直径6.8 mm、体积约1.52 cc、质量仅1.75 g,在大型动物猪模型上成功通过静脉介入手术植入到心腔内,并在右心室释放固定在心室肌上。研究团队建立了基于高分子材料构筑SICP自发电模块的方法,可兼容核磁共振检查。伴随着心脏周期性的收缩舒展SICP开路电压能够达到6.0 V,短路电流为0.2 μA,整合微型低功耗起搏芯片,实现了对房室传导阻滞疾病模型动物的有效起搏。持续3周的随访观察,SICP保持良好的起搏性能,突破了目前自供能心脏起搏器在模型动物体内植入的最长时间纪录,展示出SICP的有效性和安全性。该研究提出了一种转化心脏运动的生物机械能为电能的新方法,突破了自供能心脏起搏器的小型化和集成化挑战,为未来实现真正的“一次植入,永久工作”的无导线心脏起搏器临床应用提供了一种全新的设计理念,对进一步推动心脏起搏器的升级变革具有重要的意义。
原文链接:https://doi.org/10.1038/s41467-023-44510-6
- 四川大学杨伟教授/尹波教授团队 ACS Nano:用于压疮的泄压、监测与治疗的自供能凝胶贴片 2025-12-18
- 西工大陶凯教授 AFM:赋能人机交互界面 - 面向柔性智能系统的自供能水凝胶传感器 2025-08-17
- 安农大叶冬冬/中国药大周湘 AFM:“微流控纺丝黑科技 - 扭曲纤维素纤维开启自供能尿液监测新应用” 2024-12-10
