最近,国科温州研究院刘勇研究员、温医大附一院李圆凤博士、温医大附属口腔医院胡荣党教授团队,利用超分子逐级组装的方式构筑了一种全新的超分子光热级联纳米反应器,为生物被膜相关感染的开放性伤口的治疗提供了一条潜在的治疗方案。该研究成果发表于国际顶级期刊《Advanced Materials》。国科温州研究院博士后陈磊和研究实习员彭梦娜为第一作者。
开放性创面持续细菌感染是导致创口愈合时间延长的主要原因。细菌感染创口的临床治疗包括抗生素治疗和创面保护。然而,抗生素在临床的广泛使用为细菌提供了获得耐药性的选择压力。此外,细菌还可以通过由蛋白质、胞外细菌DNA、胞外多糖和酶组成的生物膜来保护自己免受恶劣条件或药物的攻击。生物被膜是耐药基因的储存库,促进基因水平转移。因此,以生物膜方式生长的细菌对常规抗生素的耐药性是浮游细菌的10-1000倍。60%~80%的细菌感染与创面生物膜形成有关。毫无疑问,迫切需要开发有效的非抗生素策略来应对细菌生物膜感染的创面。
近年来,许多有效的方法被应用于抗菌治疗,如化疗、光动力疗法/光催化疗法、免疫疗法、和声动力疗法。光热疗法可以利用光热剂,通过无创的光照射诱导局部热疗,进而破坏病原菌的完整性达到杀菌的目的。此外,高温还可以通过使生物被膜固有的生物活性底物(如核酸和蛋白质)失活来破坏生物被膜的稳定结构。然而,光热疗法的特异性不足,激光穿透力不足等特点限制其在抗菌领域的发展。而将光热疗法与化学动力学疗法相结合的协同治疗策略有望解决上述的问题。化学动力学疗法可以通过芬顿或类芬顿反应产生剧毒羟基自由基,通过破坏DNA、蛋白质和细胞膜诱导细菌死亡。另外,化学动力学疗法产生的活性氧可以增加细菌膜的通透性和对热的敏感性,从而达到协同抗菌作用。
基于此,本工作利用壳聚糖修饰的钯纳米立方(CPNC)、葡萄糖氧化酶(GOx)和亚铁离子(Fe2+)之间的多重氢键和配位相互作用,通过超分子策略逐级构建了光热级联纳米反应器(CPNC@GOx-Fe2+)(如图1所示)。此反应器可以整合光热治疗和化学动力学疗法对细菌进行协同杀灭,并且可以原位引发成凝实现对伤口的保护。

图1. 超分子光热纳米级联反应器CPNC@GOx-Fe2+的制备及其在促进拔牙创面愈合中的应用。
通过逐级组装的超分子光热纳米级联反应器呈现纳米方块结构,并且尺寸约为247.9纳米。其中的各组分通过透射电镜和X射线电子能谱进行了详细表征。(图2)
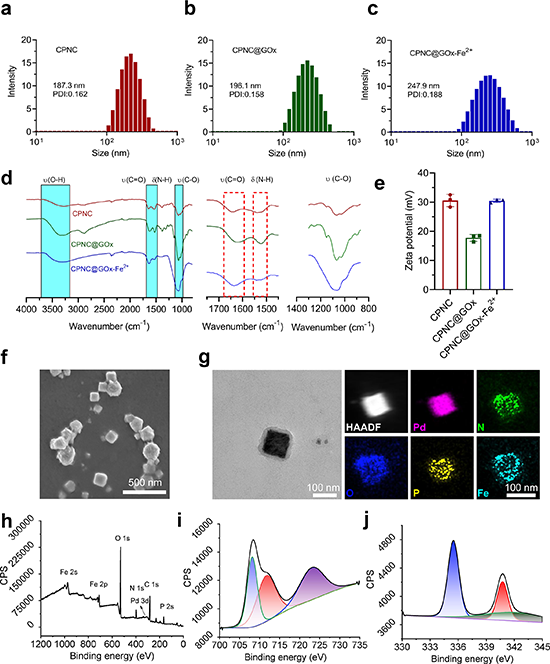
图2. 超分子光热纳米级联反应器CPNC@GOx-Fe2+的材料结构表征。
在808 nm的近红外光照下,CPNC@GOx-Fe2+展现出良好的光热效应并呈现浓度依赖性,并且具有良好的循环稳定性。通过测试米氏常数可以得知,逐级组装的过程对GOx的酶活性并没有显著的影响。在弱酸条件下,GOx协助的级联反应过程通过3,3'',5,5''-四甲基联苯胺的显色反应进行了测试并且产生的活性氧物种通过电子顺磁共振测试进一步证实为羟基自由基。(图3)

图3. 超分子光热纳米级联反应器CPNC@GOx-Fe2+的光热性能和GOx辅助的级联反应性能表征。
超分子光热纳米级联反应器CPNC@GOx-Fe2+对于变形链球菌(S. mutans)展现出良好的协同杀灭效果,并且对于S. mutans形成的成熟生物被膜也展现出良好的解离效果。(图4和图5)

图4. 超分子光热纳米级联反应器CPNC@GOx-Fe2+的体外抗菌效果评估。

图5. 超分子光热纳米级联反应器CPNC@GOx-Fe2+生物被膜去除效果的体外评价。
通过蛋白组学和全原子模拟探究了超分子光热纳米级联反应器协同抗菌的潜在机理,结果表明,超分子光热级联反应体系的潜在抗菌机制包括两个方面。首先,级联反应过程产生的·OH氧化细菌膜蛋白和磷脂双分子层,导致正常生理活动受到干扰,细胞膜结构不稳定。其次,热效应增强了细胞膜的流动性和缺陷,从而协同增强了对细菌膜上·OH的破坏。(图6和图7)

图6. 不同处理后S. mutans的蛋白质组学和代谢组学分析。
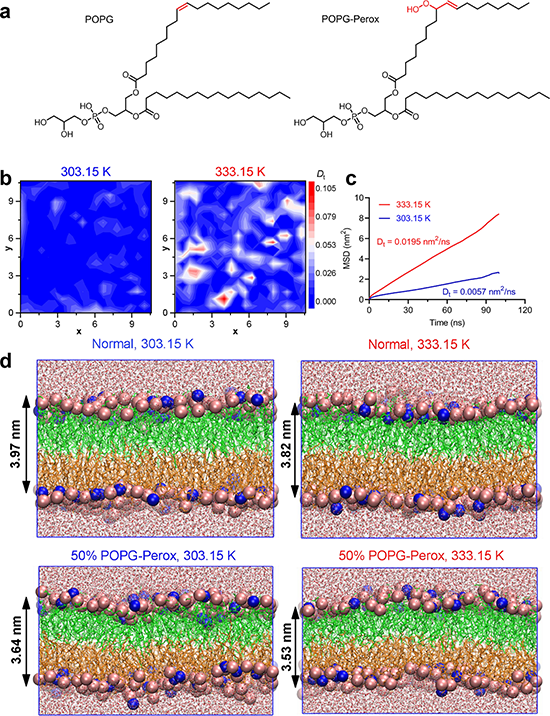
图7. 协同抗菌作用对菌膜稳定性影响的全原子分子动力学模拟。
在S. mutans生物膜相关感染拔牙创口模型中,级联反应过程产生的羟基自由基可以启动自由基聚合过程,可以在原位形成水凝胶进行创口保护。体内实验证实了CPNC@GOx-Fe2+的协同抗菌效果和创口保护性能,并且能在不影响口腔共生菌群的情况下加快感染拔牙创口愈合。(图8)

图8. 体内杀菌和口腔微生物群的评估。
此工作得到国家自然科学基金 (基金号52003184, 22103088, 82204940, 52203184和 22275043),中国博士后科学基金(基金号2022M723108)国科温州研究院启动基金(基金号WIUCASQD2021022和WIUCASQD2021019),浙江省临床检验诊断与转化研究重点实验室(基金号2022E10022)等资助支持。
文献链接:https://doi.org/10.1002/adma.202301664
刘勇研究团队介绍:
仿生聚合物组装与功能化课题组,近年来研究领域为具有生物活性的高分子材料设计、合成及自组装及其在克服细菌/癌症耐药性方面的应用。尤其专注(1)智能响应型高分子聚合物的设计、合成与表征,纳米组装体制备、分离、多功能化;(2)用于克服细菌及癌症耐药性的智能高分子聚合物纳米体系(以临床需求为导向);(3)新型高性能抗菌制剂研发与产业化。课题组近五年来在Chem. Soc. Rev., Adv. Mater. (2), Adv. Funct. Mater. (4), ACS Nano (3), Nano Today等杂志上发表一区文章30余篇,其中影响因子大于10的文章25篇。
课题组网站详见:http://wiucas.ac.cn/group/liuyong/
- 东北大学徐大可教授、李祥宇研究员团队 Angew:生物被膜框架衍生的结构自适应超滑防污防腐涂层 2025-04-14
- 北京化工大学王兴教授团队《ACS Nano》:聚(D-氨基酸)纳米粒子通过干扰葡萄球菌肽聚糖合成介导生物被膜瓦解 2024-03-13
- 北京化工大学王兴教授团队 ACS AMI:GSH/pH级联响应纳米粒子通过协同的光和化学疗法消除耐甲氧西林金黄色葡萄球菌生物被膜 2024-01-29
- 东华大学陈志钢教授团队 AFM:钙离子输送的自泵式Janus膜用于糖尿病伤口愈合 2026-04-26
- 陕科大王学川/党旭岗、温州医科大郑漫辉 AFM:可注射自修复生物质基水凝胶生物粘合剂用于伤口愈合和可穿戴生物电子一体化 2026-01-30
- 西安交大郭保林教授团队 Adv. Mater.:自适应伤口敷料用于伤口愈合与修复 2025-12-25
