金属离子可以与蛋白质结合形成金属蛋白(metalloprotein)。金属离子的存在不但影响蛋白质的多级组装,还在生命活动中起着至关重要的作用。例如二价铁离子与血红蛋白结合可以储氧载氧;铁硫蛋白作为重要的电子载体在生命活动中起着重要作用;金属酶可以催化生物体内的化学反应等。受金属蛋白启发,人们设计开发了一系列功能性金属蛋白,并在催化、生物传感器、生物电子工程等方面有广泛应用。但是设计制备金属蛋白相对复杂,成本较高。另外,高浓度重金属离子通常会造成蛋白质的不可控变性,这都限制了其大规模的应用。
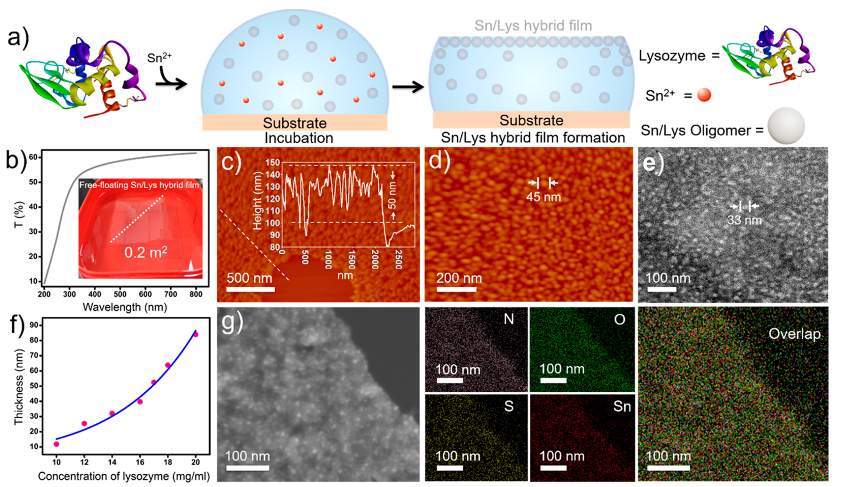
图1 锡/溶菌酶复合薄膜的制备与结构分析
面对上述问题,陕西师范大学杨鹏教授课题组提出利用二价锡离子(Sn2+)诱导蛋白质进行快速可控组装。实验中发现,与传统金属蛋白制备策略中使用钴(Co2+),镍(Ni2+),铜(Cu2+),锌(Zn2+),铁(Fe3+)等离子与蛋白形成配位作用不同,Sn2+可以高效的还原蛋白中的二硫键,并形成锡硫键(-C-S-Sn-S-C-)从而参与蛋白质组装。以溶菌酶为例,只需将一定浓度SnCl2溶液(如0.1 M)与溶菌酶溶液混合,溶菌酶分子内二硫键即可在数分钟内被还原并形成锡/溶菌酶复合物。锡/溶菌酶复合物会在气液界面快速组装,形成二维纳米薄膜。这一复合物薄膜制备方法简单,可大面积制备(面积可达0.2 m2,图1)。通过原子力显微镜,透射电子显微镜等表征可知,这一薄膜是由锡/溶菌酶复合物簇在气液界面聚集而成。由于该聚集体具有类淀粉样结构(一种自然界广泛存在的粘附体系),因此这一二维薄膜可以稳定粘附在多种基材表面并具有良好的粘附稳定性。另外,通过紫外曝光还可以得到图案化的复合物纳米薄膜(图2)。

图2 复合薄膜在多种基材表面的稳定粘附、图案化及抗菌活性。
基于锡/溶菌酶二维薄膜的特点,其展现出了多种功能性。首先,由于锡/溶菌酶簇的存在,薄膜具有优异的抗菌性能。对革兰氏阴性菌(大肠杆菌),阳性菌(金黄色葡萄球菌)以及真菌(白色念球菌)都具有良好的杀菌能力(图2)。另外,由于锡/溶菌酶簇的存在,复合薄膜还具有优异的催化性能。例如,在可见光范围内(>420nm 波长),可产生稳定的光电流。通过光催化产氢测试表明,复合薄膜具有良好的光催化水分解产氢能力(图3)。此外,复合薄膜中的锡/溶菌酶簇使复合薄膜具有良好的电子转移能力。以吡咯氧化聚合为例,除直接电催化吡咯聚合而形成聚吡咯涂层之外,在复合薄膜存在下,加入Cu2+也可催化吡咯氧化形成聚吡咯(无需外加电场),并在复合薄膜上形成聚吡咯涂层。这些进展有望应用于柔性导电材料上。
锡金属已使用上千年(如广泛使用的锡器),而以上工作证明了Sn2+可以与蛋白质结合形成类金属蛋白簇,并在界面组装为二维类淀粉样纳米薄膜。此薄膜可以粘附在多种表面形成涂层,从而赋予基材抗菌和催化等性能。
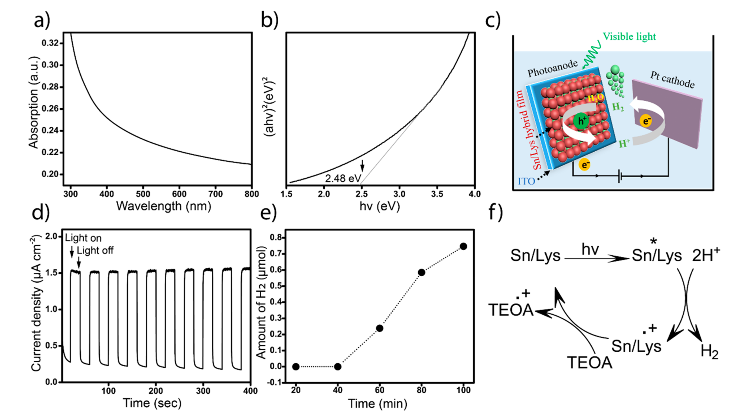
图3 复合薄膜的可见光催化活性

图4 复合薄膜的电子转移活性
由于此薄膜制备简单、成本低廉、反应迅速,为类金属蛋白的制备及组装成宏观实用材料提供了新思路,有望进行大规模使用。以上工作已在线发表在ACS Nano上(DOI: 10.1021/acsnano.9b01392),论文第一作者为来自也门的留学生Bassam Saif,通讯作者为陕西师范大学杨鹏教授和顾泉教授。该课题得到了国家自然科学基金委(Nos. 51673112, 21875132, 21872089) 等项目的资助。
论文链接:https://pubs.acs.org/doi/10.1021/acsnano.9b01392
课题组简介:
陕西师范大学化学化工学院杨鹏课题组组建于2012年底,隶属于应用表面与胶体化学教育部重点实验室。其主要学术贡献是基于蛋白质类淀粉样界面聚集与粘附,发展了一类有望代替聚多巴胺等多酚类表界面交联沉积的新的表界面粘附和化学设计新体系。已在Nature Commun. (1)、Chem. Rev. (1)、J. Am. Chem. Soc. (1)、Adv. Mater. (4)、Angew. Chem. Int. Ed. (2)等期刊发表综述和研究论文六十余篇。

- 浙江大学毛峥伟教授课题组Adv. Mater.:一种通用的聚电解质-锁定策略:从普通蛋白质到稳定的展开蛋白基粘合剂以实现快速稳健的组织密封 2025-12-25
- UCLA贺曦敏/燕山大学秦志辉、焦体峰 Adv. Mater.: 具有优异机械性能和耐久性的完全可降解蛋白质凝胶-氢键供体的调控 2025-06-27
- 华东理工刘润辉教授课题组 CCS Chem.:有效稳定蛋白质的伴侣样活性丝胶蛋白 2025-06-17
- 浙江大学徐志康/张超团队、吕朝锋团队 Adv. Mater.:超重力场作用下的异质取向纳米复合水凝胶-“以少胜多”的电磁屏蔽性能 2024-04-19
- 仰大勇教授课题组 Nano Today:细胞内DNA 纳米颗粒贯序组装实现溶酶体干扰和细胞行为调控 2024-03-14
- 天津大学仰大勇团队 Sci Adv:DNA纳米材料可控组装赋能肿瘤基因治疗 2023-09-04
