谭丽丽,杨柯,张炳春,梁勇
(中国科学院金属研究所,辽宁沈阳110016)
Study on processing and property of polyetherurethane coating on coronary stents
TAN Li-li, YANG Ke, ZHANG Bing-chun, LIANG Yong
(Institute of Metal Research, Chinese Academy of Sciences, Shenyang 110016, China)
Abstract:Dip coating method was used to prepare the polyether polyurethanes coating on coronary stents. In the light of difficulty from the complex figure of the stents, the coating processing was studied. The result showed that the coating has integrative surface, low surface roughness and desirable mechanical property, and keeps the microphase separation structure of the polyetherurethane, which ensures the blood compatibility of the coating.
Key words:coronary stent;polyether polyurethane coating;processing;property
摘要:利用浸涂方法在不锈钢冠脉支架表面制备出聚醚聚氨酯涂层。针对冠脉支架复杂的网状结构,对制备工艺进行了研究。结果表明,该涂层具有完整无缺陷的表面形貌,低的表面粗糙度,满足要求的力学性能,并保持了聚醚聚氨酯的微相分离结构,从而保证了良好的血液相容性。本项研究为探索简便而有效的支架表面涂层制备工艺奠定了基础。
关键词:冠脉支架;聚醚聚氨酯涂层;制备工艺及性能
中图分类号:TB43 文献标识码:A
文章编号:1001-9731(2004)增刊
1 引言
1987年,Sigwart首先将冠状动脉支架植入术应用于临床。近年来,我国各地的三级甲等医院也陆续开始运用这一方法,现在大约70%接受介入治疗的患者植入了支架。冠状动脉支架植入术由于有效地避免了球囊扩张后血管壁弹性回缩和血管重塑,使初始管腔扩大更为明显,再狭窄率从单纯球囊扩张年代的35%下降到18%左右。然而,支架也有局限性。支架主要是由金属材料制成的,例如不锈钢、钛、Ni-Ti形状记忆合金等。这些材料满足了结构和力学性能要求,但在生物相容性和过敏反应方面存在一些问题。支架植入后,再狭窄仍然存在,而且是制约介入性心脏病学发展的重要因素。近年来,药物支架的出现取得了令人鼓舞的成就,显著地降低了再狭窄发生率,成为这一领域的研究热点[1~4]。
在金属基体上制备聚合物涂层的方法有化学气相沉积(CVD)、离子束辅助沉积(IBAD)、浸涂等。浸涂方法具有设备简单、经济简便、适合复杂形状基体的优点。本研究结合支架自身的结构特点,选用浸涂法,对其工艺进行了系统研究。
聚醚聚氨酯具有微相分离结构,有很好的血液相容性,是医用高分子材料中综合性能相对良好的医用材料,已被用作心脏起搏器绝缘线[5]、人工血管[6,8]、介入导管[7]等直接与血液接触的医疗器械。本文研究了利用浸涂法在316L不锈钢冠脉支架上制备聚醚聚氨酯涂层,从而为药物支架的制备提供载体。
2 实验
2.1 实验材料
本实验中,316L不锈钢裸支架由中科院金属研究所提供。聚醚聚氨酯由天津聚氨酯厂提供,硅烷偶联剂及多异氰酸酯交联剂由沈阳工业学院提供,N-甲基-2-吡咯烷酮为分析纯。
2.2 实验方法
2.2.1 聚醚聚氨酯涂层的制备
将不锈钢支架清洗并化学处理后,浸入一定浓度的聚醚聚氨酯溶液中,取出后进行表面处理,于真空干燥箱内干燥。
2.2.2 涂层与基体结合力的研究
聚醚聚氨酯涂层与金属基体的粘结强度根据GB 7124-1986进行测试,所用拉力实验机为日本岛津公司的AG-5000A电子万能试验机,拉伸速率为1mm /min。
2.2.3 涂层厚度测定
在20mm×10mm×3mm的316L不锈钢薄片上利用上述工艺制备出聚醚聚氨酯涂层,利用德国QUNIS 7500 型测厚仪测定涂层厚度。
2.2.4 支架表面涂层形貌表征
将聚醚聚氨酯涂层支架表面喷金后在Camridge- S360扫描电镜下观察支架表面形貌。
2.2.5 涂层微观结构研究
涂层经环氧树脂封样,用四氧化锇染色,切片后在JEM2000FX-II型透射电镜下观察涂层微观结构。
3 结果及讨论
3.1 涂层与基体的结合力
作为体内植入用金属表面涂层,必须与金属基体具有良好的界面结合。
根据文献[9]所述,在支架膨胀后支架拐角变形及受力最大。实验中带涂层的支架经过球囊扩张3次后,拐角处表面如图1所示,表面无裂纹产生,支架内表面涂层经受与球囊的摩擦作用后无撕裂、翘起等缺陷存在,表明涂层具有良好的结合力,已经初步达到支架的使用要求。

涂层结合力包括涂层与基体的结合力以及涂层本身所具有的内聚力。实验中采用硝酸-氢氟酸对基体进行表面化学处理,在试样表面形成均匀的蚀坑,使表面粗化,提高了粘接面积。化学处理改善了金属基体与聚醚聚氨酯溶液之间的接触角,同时对基体表面起到了活化作用,使表面能与胶体之间形成化学键结合,增大了基体与涂层之间的结合力。
涂层中偶联剂的加入,在基体和有机涂层之间形成了“键桥”,以化学键的形式将二者结合起来。按胶粘理论中的化学键理论来说,化学键作用力远远超过范德华力和氢键作用力[10],因此结合力高于其它方法。当偶联剂浓度为1%时,结合力达最高值。交联剂的加入使聚醚聚氨酯涂层形成了网状交连结构,增大了涂层的内聚力。
与此同时,聚醚聚氨酯具有较强的拉伸强度,其拉伸强度是天然橡胶和合成橡胶的2~3倍,伸长率和撕裂强度也比一般橡胶要高。而且在热处理工艺中采用分段加热和后固化,保证了涂层与基体之间及涂层内部化学作用的充分进行,增加了涂层内部的交联程度,进一步提高了涂层的结合力,从而保证支架在膨胀后涂层没有发生破损。
3.2 表面形貌
植入用冠脉支架具有复杂的网状结构,利用浸涂法制备的支架表面涂层,在支架提拉过程中,会发生胶体堵塞现象,支架植入体内后将会发生严重的不良后果。图2(a)示出了未经处理的涂层后支架。图2(b)为支架提拉后经过离心处理后的表面形貌。如图可知,支架在经过离心处理后,内部没有堵塞,没有胶体粘连现象,呈现完整的网状结构。

由于支架具有复杂的网状结构,存在很大的表面张力,胶体在提拉过程中,重力无法克服表面张力作用,而使支架表面存在多余胶体。涂层提拉后经过离心处理,在离心力作用下,多余胶体从支架表面脱落,从而保持了涂层的网状结构。
与血液相接触的材料表面,粗糙度越大,暴露在血液中的面积越大,凝血的可能性越大。支架表面涂覆聚合物涂层后,在扫描电镜下观察,表面粗糙度较未涂层的不锈钢表面明显降低,如图3所示。

3.3 控制涂层厚度的工艺研究
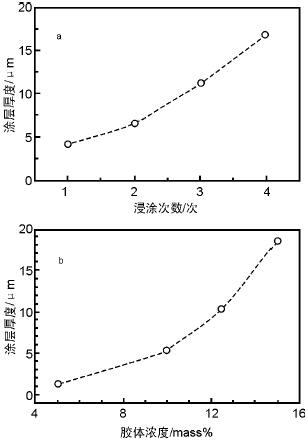
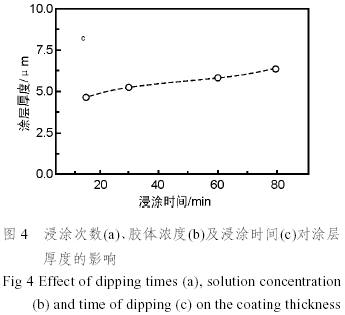
因为血管内直径很小,支架植入后占据一定空间,对血流会产生影响。对于缓释药物的聚合物涂层,也可通过涂层厚度来控制药物的携带量。涂层的厚度对于药物的释放速度及释放时间都将产生影响,因而研究支架表面涂层制备工艺时,应对涂层厚度进行控制。实验中在20mm×10mm×3mm的316L不锈钢薄片上研究了浸涂时间、浸涂次数、胶体浓度对支架表面涂层厚度的影响因素。
由图4可知浸涂时间对涂层的厚度影响非常微小,而胶体浓度和浸涂次数对涂层厚度影响较大。其中胶体浓度对支架表面涂层形貌会产生影响,因为支架复杂的网状结构,当胶体浓度过大时,涂层将阻塞网状支架。由实验可知,当胶体浓度在10%w/w以下时,胶体可以顺利通过支架网,容易形成完整的支架表面涂层。由此,可以在胶体浓度及浸涂时间确定时,通过浸涂次数控制涂层的厚度。
3.4 涂层微观结构
聚醚聚氨酯由软段和硬段两部分构成,由于这两部分无相容性,因而形成了微相分离结构。很多研究结果表明[11],血管壁内皮具有微观非均相结构,因此,聚氨酯所具有的微相分离结构对材料的抗凝血性能有重要作用。图5为聚醚聚氨酯原料(a)及本研究所制备的聚醚聚氨酯涂层(b)的内部结构图片,由图可见,添加偶联剂、交联剂及经过相应的热处理之后,聚醚聚氨酯的内部微相结构未受到破坏,从而保证了支架表面聚醚聚氨酯涂层的血液相容性。

4 结论
实验采用浸涂工艺,制备出具有连续、完整的冠脉支架表面聚醚聚氨酯涂层。涂层具有较低的表面粗糙度,保持了聚醚聚氨酯的微相分离结构。实验还研究了影响涂层厚度的因素,确定了控制涂层厚度的工艺方法。通过膨胀实验表明,涂层满足支架使用的力学性能要求。本项研究为探索简便而有效的支架表面涂层制备工艺奠定了基础。
参考文献:
[1] Yoon Ki Joung, Hyun Il Kim, Sung Soo Kim, et al. Estrogen release from metallic stent surface for the prevention of restenosis, Journal of Controlled Release [J]. International Journal of Cardiology, 2003,92,83-91.
[2] Garas Samer M, Huber Philip, Scott Neal A. Overview of therapies for prevention of restenosis after coronary interventions, Pharmacol therapeut [J]. 2001,92, 165-178.
[3] Lewis A. L, Tolhurst L. A, Stratford P. W. Analysis of a phosphorylcholine-based polymer coating on a coronary stent pre- and post-implantation, Biomaterials [J]. 2002,23(7), 1697-1706.
[4] Swanson Neil, Hogrefe Kai, Javed Qamar, et al. In vitroevaluation of vascular endothelial growth factor, (VEGF)- eluting stents, International of cardiology [J]. 2003, 92(2-3): 247-251.
[5] Pinchuk L, A review of the biostability and carcinogenicity of polyurethanes in medicine and the new-generation of biostable polyurethanes [J]. Journal of biomaterials science-polymer eition, 1994,6(3), 225-267.
[6] Stokes K, Urbanski P, Upton J., The in vivo auto-oxidation of polyether polyurethane by metal ions [J]. Journal of biomaterials science-polymer eition, 1990,1(3): 207-230.
[7] Hess F, Jerusalem C, Braun B., A fibrous polyurethane microvascular prosthesis [J]. J. Cardiovas Surg., 1983, 24: 509-515.
[8] Spilezewski K L., Anderson J M, et al., In vivo biocompa- tibility of catheter materials [J]. Biomaterials, 1988, 9: 253-256.
[9] 黄远, 李林安, 刘文西. 医用心血管支架的非线性有限元分析[J].中国生物医学工程学报, 2003, 22(2): 139-148.
[10] 李子东编. 实用粘接手册,[M]. 上海科学技术文献出版社, 1991年,366.
[11] 顾汉卿编. 生物医学材料学,[M]. 天津: 天津科技翻译出版社,chap.6.
基金项目:国家863项目(2001AA320604)
作者简介:谭丽丽(1977-),女,博士生,从事生物材料及器件的研究。
论文来源:中国功能材料及其应用学术会议,2004年,9月12-16日