Current Location :> Home > News > Text
Moderate Li+-Solvent Binding for Gel Polymer Electrolytes with Stable Cycling toward Lithium Metal Batteries
【研究背景】锂金属电池(LMBs)因其高能量密度被视为下一代储能设备。然而,目前的电解质体系在溶剂化调控方面存在不足,导致了缓慢的锂离子传输和不可控的锂枝晶生长,限制了锂金属电池应用。通过降低Li+与溶剂的亲和力而形成的弱溶剂化环境有利于改善LMBs电解质的性能。这是因为当阴离子进入Li+溶剂化鞘内时,将会形成由阴离子衍生的富含无机组分的固态电解质界面(SEI)。然而,弱溶剂化调控难免对锂盐解离产生影响,导致电解质的离子电导率降低,从而影响电解质的离子传输性能。因此,如何合理调节溶剂化以实现锂离子的快速传输和稳定的固态电解质界面(SEI)之间的平衡对优化电池稳定性能至关重要。
【工作简介】近日,武汉理工大学木士春、曾炜豪团队及廖小彬博士等研究者通过原位聚合策略设计并构建了三种具有高、中、低Li+-溶剂结合强度的凝胶聚合物电解质(GPEs)。其中,具有中等Li+-溶剂结合强度的凝胶聚合物电解质(MB-GPE)促进了阴离子衍生的溶剂化结构,形成了富含无机成分(如LiF)的SEI,有效抑制了界面副反应,并加速了界面反应动力学。此外,MB-GPE对锂盐解离的影响较小,具有优异的离子电导率。相比之下,具有高和低Li+-溶剂结合强度的GPEs在LMBs中表现出较差的循环性能。这主要是由于SEI稳定性和Li+传输受到显著限制。研究证实,设计具有中等Li+-溶剂结合强度的凝胶聚合物电解质是一种有效策略,能够实现快速的Li+传输并促进稳定SEI层的形成,从而确保锂金属电池的高比容量和长期稳定性。该文章发表在国际顶级期刊Energy & Environmental Science上。张少杰和李忠澎为本文共同第一作者。
【内容表述】在这项工作中,为了探寻溶剂化调控与电解质性能之间的关系,作者采用原位聚合策略设计、构建了具有不同Li+-溶剂结合力的GPEs。他们合成了三组具有不同氟化组分的凝胶电解质,即碳酸乙烯酯(EC)和碳酸甲乙酯(EMC)、氟化碳酸乙烯酯(FEC)和2,2,2-三氟乙基碳酸甲酯(FEMC)及二氟碳酸乙烯酯(DFEC)和FEMC,分别具有高Li+-溶剂结合力(HB-GPE)、中等Li+-溶剂结合力(MB-GPE)和低Li+-溶剂结合力(LB-GPE)。在本项工作中,与锂金属具有良好相容性的聚乙二醇二丙烯酸酯(PEGDA)被选择作为聚合单体。
3.1 凝胶聚合物电解质的设计在具有高Li+-溶剂结合力的凝胶电解质(HB-GPE)中,由于溶剂较强的亲和力,锂盐可实现充分解离。但溶剂过多地进入Li+的溶剂化鞘中时,在迁移至金属锂表面时容易生成含大量有机组分的SEI,而且锂枝晶生长亦较快,不利于锂金属的稳定循环。而在具有低Li+-溶剂结合力的凝胶电解质(LB-GPE)中,由于溶剂的溶剂化能力较差,Li+仍与阴离子紧密结合,大量锂盐未解离,导致离子电导率大幅降低。但由于较多的阴离子可迁移至Li+的溶剂化鞘中,界面性能有所改善。在具有适度Li+-溶剂结合力的凝胶电解质(MB-GPE)中,由于溶剂具有适度亲和力,Li+既能摆脱阴离子的束缚,锂盐得到充分解离,赋予电解质高的离子电导率,阴离子也能顺利迁移至Li+的溶剂化鞘中,从而衍生出由阴离子主导且富含无机组分(例如LiF)的SEI,可有效抑制锂枝晶的生长。在实现金属锂的高稳定循环的同时,还可实现锂离子的快速迁移。
本工作首先对三种具有不同Li+-溶剂结合的凝胶聚合物电解质进行了模拟计算。从EC到FEC再到DFEC,Li+与不同溶剂的结合力数值从-2.2降至-2.0 eV,再降至-1.81 eV。此外,从EMC到FEMC,结合力数值从-2.0降至-1.66 eV。计算结果表明,随着氟化程度的增加,Li+-溶剂结合力逐渐降低。采用分子动力学(MD)模拟分析Li+-溶剂结合力与溶剂化结构之间的关系。在第一溶剂化鞘层(r=2 ?)中,对于HB-GPE,Li+与EC的配位数为0.4,Li+与EMC的配位数为0.29;对于MB-GPE,Li+与FEC的配位数为0.19,Li+与FEMC的配位数为0.06;对于LB-GPE,Li+与DEFC的配位数为0.08,Li+与FEMC的配位数为0.1。因此,随着凝胶电解质中Li+与溶剂结合力的减少,在第一溶剂化鞘中,Li+/溶剂的总配位数逐渐减少,而Li+/TFSI-的配位数逐渐增加。径向分布函数(RDFs)结果进一步证实,随着溶剂分子氟化程度的增加,在第一溶剂化鞘层(r=2 ?)中,Li+与溶剂分子的相互作用逐渐减弱(EC>FEC>DFEC,EMC>FEMC),更多的阴离子进入到Li+的溶剂化结构中,有利于形成由阴离子衍生的富含无机物的SEI。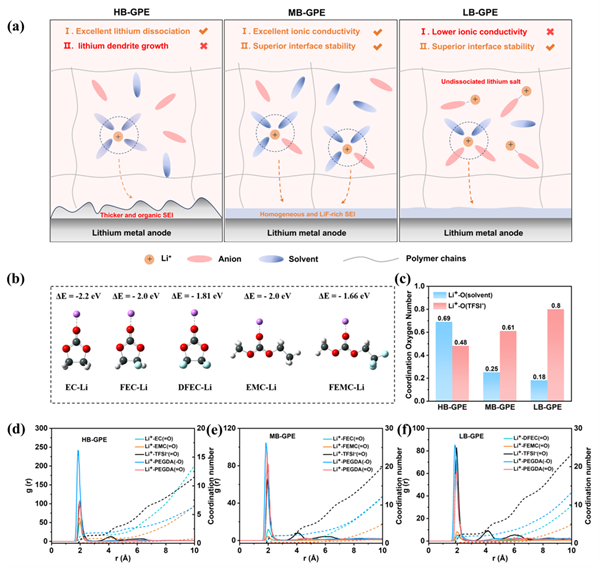 图1 凝胶聚合物电解质设计和溶剂化结构研究。(a) HB-GPE、MB-GPE和LB-GPE的溶剂化结构和SEI演变过程。(b) 不同溶剂与Li+的结合力计算。(c) 不同凝胶电解质中Li+与溶剂和TFSI-的氧原子配位数变化。(d,e,f)由MD模拟得到的HB-GPE、MB-GPE和LB-GPE的径向分布函数。
图1 凝胶聚合物电解质设计和溶剂化结构研究。(a) HB-GPE、MB-GPE和LB-GPE的溶剂化结构和SEI演变过程。(b) 不同溶剂与Li+的结合力计算。(c) 不同凝胶电解质中Li+与溶剂和TFSI-的氧原子配位数变化。(d,e,f)由MD模拟得到的HB-GPE、MB-GPE和LB-GPE的径向分布函数。
3.2 物化性能评估采用密度泛函理论(DFT)对三种凝胶聚合物电解质所使用的溶剂和锂盐的最高占据分子轨道(HOMO)能级和最低未占据分子轨道(LUMO)能级计算。从EC到FEC,再到DFEC,HOMO和LUMO能值逐渐降低;从EMC到FEMC,HOMO和LUMO能值也逐渐降低。LiTFSI的LUMO能级最低(-1.43 eV),更有利于在锂阳极处被还原分解,形成富含LiF无机组分的SEI。
通过Raman拉曼光谱和液态核磁NMR测试分析Li+在HB-GPE、MB-GPE和LB-GPE的溶剂化结构中的解离状态。LiTFSI的光谱可拟合成三个部分:自由TFSI-(位于738.9 cm-1,未配位的TFSI-)、接触离子对(CIP,742.7 cm-1,与一个Li+结合的TFSI-)和聚集体(AGG,747.9 cm-1,与两个或更多Li+结合的TFSI-)。LB-GPE中存在少量游离TFSI-信号,表明LB-GPE中存在大量未解离的Li+。MB-GPE中存在较多的游离TFSI-信号和CIP信号,表明锂盐已充分解离,有利于形成由阴离子主导的溶剂化结构。进一步采用7Li NMR分析溶剂化结构中Li+周围的化学环境。与HB-GPE相比,MB-GPE和LB-GPE的7Li峰向左移,表明Li+周围的电荷屏蔽程度降低,有利于锂离子的快速迁移。这证明具有适度Li+-溶剂结合力的MB-GPE可同时实现LiTFSI的完全解离和Li+的快速迁移。虽然HB-GPE具有最佳的锂解离状态,但锂离子迁移受阻;而低Li+-溶剂结合力的LB-GPE则会大幅阻碍LiTFSI的解离。
测试结果表明,MB-GPE在室温下具有高的离子电导率(1.95×10-3 S cm-1),居于LB-GPE(6.73×10-4 S cm-1)和HB-GPE(3.84×10-3 S cm-1)之间。MB-GPE的迁移活化能(0.151 eV)略高于LB-GPE的0.143 eV,而低于HB-GPE(0.193 eV)。锂离子迁移势垒的降低有利于Li+快速迁移。MB-GPE和LB-GPE的氧化电位分别为5.12 V和5.23 V,高于HB-GPE的4.08 V,表明MB-GPE拥有高的抗氧化性能。在4.2至4.7 V的电压范围内,使用MB-GPE和LB-GPE的Li||NCM811电池均出现稳定的漏电流,表现出优异的高压稳定性。而使用HB-GPE的电池在恒压充电至4.3 V时电流显著增加,表明在4.3 V高压下HB-GPE的稳定性较差。此外,MB-GPE的Li+迁移数为0.62,分别高于HB-GPE(0.58)和LB-GPE(0.31)。较高的Li+迁移数表明MB-GPE的界面极化较低,降低了浓差极化的影响,从而促进锂的均匀沉积。 图2 HB-GPE、MB-GPE和LB-GPE物化特性。(a) EC、EMC、FEMC、FEC、DFEC和LiTFSI的HOMO和LUMO能级。(b) MB-GPE、LiTFSI、FEMC、FEC和PEGDA傅立叶变换红外光谱,波长范围为500-2500 cm-1。(c) HB-GPE、MB-GPE和LB-GPE的拉曼光谱。(d) HB-GPE、MB-GPE和LB-GPE的7Li NMR光谱。(e) HB-GPE、MB-GPE和LB-GPE离子电导率。(f) HB-GPE、MB-GPE和LB-GPE的阿伦尼乌斯拟合。(g) HB-GPE、MB-GPE和LB-GPE的LSV曲线。(h) MB-GPE电化学浮动分析。(i) 使用MB-GPE的锂对称电池的极化曲线。插图显示极化前后的奈奎斯特图。(j) MB-GPE/PP复合隔膜的杨氏模量图。(k) HB-GPE和MB-GPE可燃性测试。
图2 HB-GPE、MB-GPE和LB-GPE物化特性。(a) EC、EMC、FEMC、FEC、DFEC和LiTFSI的HOMO和LUMO能级。(b) MB-GPE、LiTFSI、FEMC、FEC和PEGDA傅立叶变换红外光谱,波长范围为500-2500 cm-1。(c) HB-GPE、MB-GPE和LB-GPE的拉曼光谱。(d) HB-GPE、MB-GPE和LB-GPE的7Li NMR光谱。(e) HB-GPE、MB-GPE和LB-GPE离子电导率。(f) HB-GPE、MB-GPE和LB-GPE的阿伦尼乌斯拟合。(g) HB-GPE、MB-GPE和LB-GPE的LSV曲线。(h) MB-GPE电化学浮动分析。(i) 使用MB-GPE的锂对称电池的极化曲线。插图显示极化前后的奈奎斯特图。(j) MB-GPE/PP复合隔膜的杨氏模量图。(k) HB-GPE和MB-GPE可燃性测试。
3.3 金属锂界面稳定性分析使用HB-GPE、LB-GPE和MB-GPE等三种凝胶聚合物电解质组装了Li||Li对称电池,对金属锂在锂沉积和剥离过程中的界面稳定性进行评估。测试电流密度为0.5 mA cm-2,容量为0.5 mAh cm-2。Li|MB-GPE|Li对称电池稳定循环超过3200小时后仍保持约30 mV的低过电位,具有优异的循环稳定性能。相比之下,使用HB-GPE和LB-GPE的Li||Li对称电池在循环900小时和1367小时后分别出现短路,极化电压骤减,表明此时金属锂发生严重副反应,界面稳定性较差。进一步测试临界电流密度(CCD)以评估HB-GPE、LB-GPE和MB-GPE抑制锂枝晶的能力。MB-GPE的CCD为3.5 mA/cm2,而HB-GPE和LB-GPE的CCD分别为1.5和2 mA/cm2。这表明MB-GPE可承受更大的电流密度,在抑制锂枝晶生长方面的能力最强。
分别使用HB-GPE、LB-GPE和MB-GPE组装了Li||Cu电池,进一步考察其锂沉积和剥离过程中的库仑效率(CE)。使用MB-GPE和LB-GPE的锂铜电池的平均CE值分别为93.42%和93.64%,均高于HB-GPE(65.97%)。使用MB-GPE的Li||Cu电池在循环第1、50和150圈时的极化电压分别为82、40和46 mV。较小的极化电压表明MB-GPE在锂沉积-剥离过程中具有出色的稳定性。而使用HB-GPE的Li||Cu电池在循环第1和50圈时的极化电压分别为108和99 mV,随后库伦效率迅速降低。使用LB-GPE的Li||Cu电池在循环第1、50和150圈时的极化电压分别为134、97和161 mV。其较大的极化电压与其较差的锂沉积形态相对应。进一步分析铜箔表面沉积的锂的形态和厚度可知,在使用HB-GPE的铜箔上可观察到疏松多孔的针状锂枝晶,表明HB-GPE与锂金属发生了严重的副反应,并产生大量死锂;当使用MB-GPE时,铜箔上沉积的锂表面平整致密,没有可见的枝晶;当使用LB-GPE时,沉积在铜箔上的锂呈现出带有凹坑的块状形态,表明存在不均匀的锂沉积。截面SEM观察结果表明,使用MB-GPE和LB-GPE后的沉积锂的厚度分别为16.8和16.9 μm,小于HB-GPE的48.6 μm。这表明MB-GPE能够促进锂离子通量的均匀分布并调节锂成核,最终实现锂的均匀沉积。 图3 锂沉积/剥离性能评估和锂沉积形态表征。(a)基于HB-GPE、MB-GPE和LB-GPE的Li||Li对称电池在0.5 mA cm-2和0.5 mAh cm-2条件下的循环性能。(b)本研究中的GPE与最近报道的其他GPE在离子电导率和对锂稳定性方面的比较。(c)Li|MB-GPE|Li对称电池的临界电流密度测试。(d)电流密度为0.2 mA cm-2、容量为0.2 mAh cm-2时锂在铜箔上的沉积/剥离库仑效率。(e)基于MB-GPE的Li||Cu电池的电压-容量曲线,插图显示了第1、50和150圈时的电压-容量曲线。在基于(f)HB-GPE、(g)MB-GPE和(h)LB-GPE电池中,在1 mA cm–2和5 mAh cm–2条件下锂在铜箔表面的沉积形貌;插图是使用HB-GPE、MB-GPE和LB-GPE后锂沉积的横截面形态。
图3 锂沉积/剥离性能评估和锂沉积形态表征。(a)基于HB-GPE、MB-GPE和LB-GPE的Li||Li对称电池在0.5 mA cm-2和0.5 mAh cm-2条件下的循环性能。(b)本研究中的GPE与最近报道的其他GPE在离子电导率和对锂稳定性方面的比较。(c)Li|MB-GPE|Li对称电池的临界电流密度测试。(d)电流密度为0.2 mA cm-2、容量为0.2 mAh cm-2时锂在铜箔上的沉积/剥离库仑效率。(e)基于MB-GPE的Li||Cu电池的电压-容量曲线,插图显示了第1、50和150圈时的电压-容量曲线。在基于(f)HB-GPE、(g)MB-GPE和(h)LB-GPE电池中,在1 mA cm–2和5 mAh cm–2条件下锂在铜箔表面的沉积形貌;插图是使用HB-GPE、MB-GPE和LB-GPE后锂沉积的横截面形态。
3.4 锂金属电池的循环性能分析以磷酸铁锂(LiFePO4)为正极,锂金属为负极,组装成Li||LiFePO4锂金属电池,并测试电池在不同倍率下的循环性能。Li|MB-GPE|LiFePO4电池在0.5 C下的初始放电比容量为144.6 mAh g-1;在循环780圈后,其放电比容量为122 mAh g-1,平均CE值为99.99%,容量保持率为84.4%。相比之下,Li|HB-GPE|LiFePO4和Li|LB-GPE|LiFePO4的初始放电比容量分别为126.7和139.7 mAh g-1,循环500圈后的容量保持率分别为46.8%和72.3%。Li|MB-GPE|LiFePO4电池在更大倍率(1 C)下仍具有优异的循环性能。
为了评估MB-GPE与高镍正极材料(NCM811)的兼容性,组装了Li||NCM811锂金属电池,并在3.0-4.3 V的电压范围内测试其循环性能。使用MB-GPE的Li||NCM811电池在0.5 C下的初始放电比容量为157 mAh g-1。在循环400圈后,其放电比容量降至125.8 mAh g-1,但容量保持率仍高达80.1%。而Li|LB-GPE|NCM811电池的初始放电比容量为135.8 mAh g-1,循环230次后容量保持率降为52.1%。值得注意的是,仅仅循环10次后,Li|HB-GPE|NCM811电池的放电比容量就从145.2下降到77.5 mAh g-1,难以在高电压下正常工作。这个测试结果也与HB-GPE较低的电化学窗口和较差的电化学浮动测试结果相对应。为了进一步证明MB-GPE在实际应用中的潜力,进一步将其与高负载的NCM811正极片(负载量:9.2 mg cm-2)和超薄的锂箔负极(厚度:50 μm)组装成软包电池。软包电池在0.2 C倍率下可稳定循环20个周期,容量保持率为84%,并表现出优越的安全性能。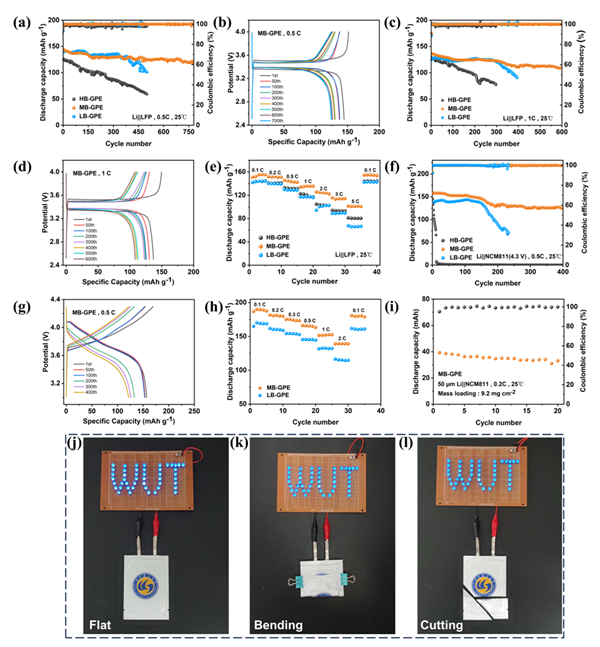 图4 基于HB-GPE、MB-GPE和LB-GPE电池的锂金属电池循环性能。(a) 基于三种凝胶聚合物电解质的Li||LFP电池在0.5 C下的循环性能。(b)基于MB-GPE的Li||LFP电池在0.5 C倍率,4 V截止电压下的放电/充电电压曲线。(c) 基于三种凝胶聚合物电解质的Li||LFP电池在1 C下的循环性能。(d) 基于MB-GPE的Li||LFP电池在1 C倍率,4 V截止电压下的放电/充电电压曲线。(e)基于三种凝胶聚合物电解质的Li||LFP电池的倍率性能,以及(f)Li||NCM811电池在0.5 C下的循环性能。(g)基于MB-GPE的Li||NCM811电池在0.5 C倍率,4.3 V截止电压下的放电/充电电压曲线。(h)基于三种凝胶聚合物电解质的Li||NCM811电池的倍率性能。(i)基于MB-GPE的Li||NCM811软包电池的循环性能。基于MB-GPE的Li||NCM811软包电池在不同状态的安全测试:(j)铺展;(k)弯折;(l)剪切。
图4 基于HB-GPE、MB-GPE和LB-GPE电池的锂金属电池循环性能。(a) 基于三种凝胶聚合物电解质的Li||LFP电池在0.5 C下的循环性能。(b)基于MB-GPE的Li||LFP电池在0.5 C倍率,4 V截止电压下的放电/充电电压曲线。(c) 基于三种凝胶聚合物电解质的Li||LFP电池在1 C下的循环性能。(d) 基于MB-GPE的Li||LFP电池在1 C倍率,4 V截止电压下的放电/充电电压曲线。(e)基于三种凝胶聚合物电解质的Li||LFP电池的倍率性能,以及(f)Li||NCM811电池在0.5 C下的循环性能。(g)基于MB-GPE的Li||NCM811电池在0.5 C倍率,4.3 V截止电压下的放电/充电电压曲线。(h)基于三种凝胶聚合物电解质的Li||NCM811电池的倍率性能。(i)基于MB-GPE的Li||NCM811软包电池的循环性能。基于MB-GPE的Li||NCM811软包电池在不同状态的安全测试:(j)铺展;(k)弯折;(l)剪切。
3.5 电极界面分析基于三种凝胶聚合物电解质的Li||LiFePO4电池在0.5 C下循环20次后,进一步采用X射线光电子能谱(XPS)对其锂金属表面进行深度蚀刻,以分析SEI组分。在C 1s光谱中,基于HB-GPE和LB-GPE电池的金属锂表面含有大量的C-O和C=O有机成分,且随着刻蚀深度的增加,C-O和C=O有机成分仍大量存在。这表明基于HB-GPE和LB-GPE电池的金属锂发生了严重的副反应,从而产生较多有机组分。相反,基于MB-GPE电池的金属锂中,可以观察到少量的C-O和C=O成分,且随刻蚀深度增加,含量逐渐减少;此外,金属锂中的Li2CO3无机成分较多,含量分布均匀。在O1s光谱中,与HB-GPE和LB-GPE相比,随着蚀刻深度的增加,基于MB-GPE电池的SEI层中观察到了Li2O无机组分,但没有发现RO-Li有机成分。在F1s光谱中,与HB-GPE和LB-GPE相比,基于MB-GPE电池的金属锂表面仅含有LiF无机氟化物,表明形成了富含Li2CO3、Li2O、LiF等无机组分的SEI层。多种无机组分的协同作用,提高了电池的电化学稳定性,抑制了锂枝晶生长,并构筑了均匀的Li+扩散通量,赋予了锂金属负极高的循环寿命。
基于MB-GPE电池,进一步采用了飞行时间二次离子质谱法(TOF-SIMS)探究其SEI中无机组分的三维含量分布。随着溅射时间的增加,基于HB-GPE电池的金属锂中C2HO-有机组分的含量始终多于LiF2-,无机组分占少量。与HB-GPE相比,基于MB-GPE电池的薄SEI层中同时富含LiF2-(来自LiF)、Li2CO3-和LiO2-离子;而且C2HO-有机组分的含量低于LiF2-,无机组分占主导。这些研究结果表明,MB-GPE促进了富含Li2CO3、Li2O和LiF无机成分的SEI层的形成,有利于抑制锂枝晶的生长,从而实现锂金属电池的长期稳定循环。 图5 SEI层的界面化学分析:基于(a)HB-GPE、(b)LB-GPE和(c)MB-GPE电池的锂金属阳极循环20次后C 1s的XPS深度分析;基于(d)HB-GPE、(e)LB-GPE和(f)MB-GPE电池的锂金属阳极循环20次后O 1s的XPS深度分析;基于(g)HB-GPE、(h)LB-GPE和(i)MB-GPE电池的锂金属阳极循环20次后F 1s的XPS深度分析。基于(j)HB-GPE和(k)MB-GPE电池的锂金属表面的代表性二次离子的TOF-SIMS二维和三维映射图像。
图5 SEI层的界面化学分析:基于(a)HB-GPE、(b)LB-GPE和(c)MB-GPE电池的锂金属阳极循环20次后C 1s的XPS深度分析;基于(d)HB-GPE、(e)LB-GPE和(f)MB-GPE电池的锂金属阳极循环20次后O 1s的XPS深度分析;基于(g)HB-GPE、(h)LB-GPE和(i)MB-GPE电池的锂金属阳极循环20次后F 1s的XPS深度分析。基于(j)HB-GPE和(k)MB-GPE电池的锂金属表面的代表性二次离子的TOF-SIMS二维和三维映射图像。
【核心结论】本项工作中,研究员人员设计、合成了具有适度Li+-溶剂结合力的含氟凝胶聚合物电解质(MB-GPE),并系统评估了具有高、适中、低Li+-溶剂结合力凝胶聚合物电解质的电化学性能。结果表明,引入氟化溶剂FEC和FEMC的MB-GPE能有效地平衡弱溶剂化调控和锂离子传输之间的矛盾;此外,该电解质还有助于形成富含LiF等无机组分的SEI,极大改善了锂金属负极的循环性能。MB-GPE具有1.95×10-3 S cm-1的高离子电导率、0.62的锂离子迁移数和5.12 V的宽电化学窗口。基于MB-GPE的Li||Li对称电池在0.5 mA cm-2的电流密度下实现了超过3200小时的稳定循环,而Li|MB-GPE|Cu电池在0.2 mA cm-2的电流密度下展现出优异的锂沉积/剥离性能和高的库伦效率(93.42%)。当MB-GPE应用于LiFePO4和NCM811多种正极的锂金属电池时,其循环可逆性显著提高。此外,使用MB-GPE组装的Li||NCM811软包电池具有良好的循环性能和优异的安全性能。本工作所提出的溶剂化结构策略为设计高性能凝胶聚合物电解质及高性能固态电池的开发提供了一个新的思路。
【文献详情】Shaojie Zhang#, Zhongpeng Li#, Yixin Zhang, Xuanpeng Wang, Peiyang Dong, Saihai Lei, Weihao Zeng*, Juan Wang, Xiaobin Liao*, Xingye Chen, Dongqi Li, Shichun Mu*. Moderate Li+-Solvent Binding for Gel Polymer Electrolytes with Stable Cycling toward Lithium Metal Batteries. Energy & Environmental Science, 2025, Doi:10.1039/D4EE05866F.