- 吉林大学赵杰等《ACS Sustain. Chem. Eng.》封面:可见光调控多巴胺介导快速构建金属有机骨架膜及抗菌性能研究
- 来源:赵杰教授个人网站 2020-10-29
金属有机骨架(MOFs)作为一种典型的具有高表面积、可调控孔尺寸以及丰富物理化学性质的晶体材料已得到广泛应用。材料表面上组装MOFs在拓展其应用方面具有独特的优势。然而,制备MOF膜仍然是一项具有挑战性的工作,其过程繁琐而复杂。近日,吉林大学工程仿生教育部重点实验室任露泉院士团队赵杰副教授课题组报道了一种利用可见光照,即可在多巴胺(DA)共存体系下将UiO-66粒子组装在基底表面,该方法不仅具有高效、快速、普适性强等优点,还可避免传统DA组装需在紫外、氧化性、弱碱性等环境的缺点。
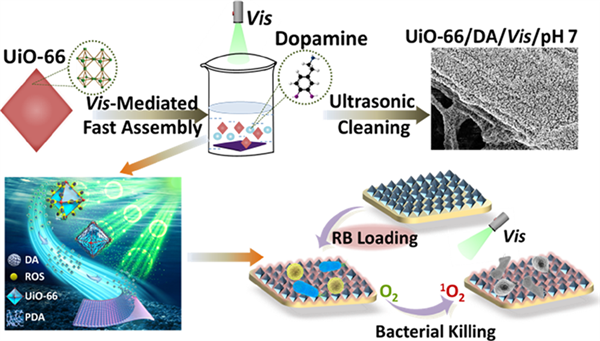
在该体系中,可见光、多巴胺(DA)与待组装粒子UiO-66具有协同效应:可见光诱导UiO-66产生活性氧(ROS),ROS促进多巴胺聚合,而聚多巴胺(PDA)又可协助UiO-66粒子在表面组装,形成致密、均匀且稳定的MOF膜,强力超声处理后仍保持其表面形态。借助MOF膜吸附能力,将光敏剂孟加拉红(RB)引入MOF膜后,所得到的复合膜展现出对革兰氏阳性金黄色葡萄球菌(S. aureus)和革兰氏阴性大肠杆菌(E. coli)的快速光动力杀菌效果(图1)。该研究成果以“Formation and Antibacterial Performance of Metal?Organic Framework Films via Dopamine-Mediated Fast Assembly under Visible Light”(ACS Sustain. Chem. Eng. 2020, 8, 42, 15834–15842)为题发表在了国际著名期刊ACS Sustainable Chemistry & Engineering,并被选为杂志当期正封面。
与采用多巴胺协助组装纳米颗粒或对基底表面进行预修饰的常规方法不同,该“一步法”实现了在反应体系中性(pH=7),短时间内(4 h)UiO-66在材料表面的组装(图2)。该方法既发挥多巴胺固有的强粘附力与实验方法简便的优点,可见光与待组装粒子的协同作用又打破了传统多巴胺反应耗时冗长、需要碱性介质等反应条件的限制。
该工作中提出了基于“多巴胺敏化效应”的薄膜构建机理,即多巴胺作为电子转移介质将光生电子转移到金属有机框架的导带,使表面的氧还原得到ROS(超氧阴离子),生成的ROS在pH值为7的中性环境下引发多巴胺适度聚合,避免多巴胺自身快速聚合形成聚集体,提高了多巴胺利用效率,保证多巴胺作为“粘结剂”将MOFs固定在基底表面,促进MOFs在基底上的组装(图3)。此外,选用UV光照射产生大量ROS促进多巴胺快速聚合或者利用捕获剂清除体系中ROS,探究体系中ROS产量对多巴胺聚合与UiO-66组装的影响。实验结果表明大量ROS产生并不利于多巴胺协助粒子在表面的组装,而缺少ROS多巴胺则无法在中性条件下快速聚合。
光敏剂是光动力学杀菌的重要构成要素。利用MOF膜吸附性能,该工作中将在可见光下能够稳定产生具有杀菌效果的单线氧1O2的光敏剂孟加拉红(RB)成功引入到MOF膜(图4)。所制备的抗菌复合膜展现出出众的光动力杀菌效果,可见光下仅需5分钟,对两种试验细菌(S. aureus与E. coli)杀菌率即可达到99.9%(图5、6)。图 4. (a-b) MOF膜吸附性能表征与(c)可见光下抗菌复合膜单线氧产率测定.图 5. MOF复合膜抗菌实验结果图6. MOF复合膜抗菌效果对比与光动力杀菌示意图.此项工作提供了一种可见光调控、多巴胺介导的快速一步组装MOF膜的策略,缩短了反应时间,兼具反应条件温和的独特优势,且赋予了材料优异的抗菌性能,为在不同材料表面组装MOF膜提供了新的思路。
该论文第一作者为郝凌婉博士,赵杰副教授为通讯作者。

- [来源:中国聚合物网]
- 了解更多请进入: 赵杰教授个人网站